稳定型氟代S-腺苷甲硫氨酸类似物实现酶促氟甲基化
氟在药物化学和农业化学中发挥着非常重要的作用。通过向化合物分子中引入氟原子,可以显著改善化合物的代谢稳定性、亲脂性和生物活性。氟烷基化是向化合物分子中引入氟的一种有效方法。其中,氟甲基 (CH2F) 由于可以作为多种官能团的生物电子等排体而成为非常重要的氟烷基官能团。然而, 自然界可以引入氟及含氟基团的酶很少, 而区域特异性地向化合物分子中引入氟甲基是有机化学中的一大挑战。近日,天津大学董敏(点击查看介绍)课题组以甲基转移酶的天然辅因子S-腺苷甲硫氨酸 (SAM) 出发,设计合成了一种稳定的氟代SAM类似物:氟代脱羧SAM (F-dcSAM)。F-dcSAM可以被多种O-、S-和N-甲基转移酶识别而成为一种通用的生物氟甲基化试剂,高区域选择性地氟甲基化多个活性药物分子。动力学研究表明,对于甲基转移酶NtCOMT和DnrK,F-dcSAM是近似甚至优于SAM的更好的底物。F-dcSAM还可以通过卤素甲基转移酶(HMT)制得,由HMT和甲基转移酶组成的双酶级联反应可以通过原位循环生成F-dcSAM实现氟甲基化产物的高效制备。
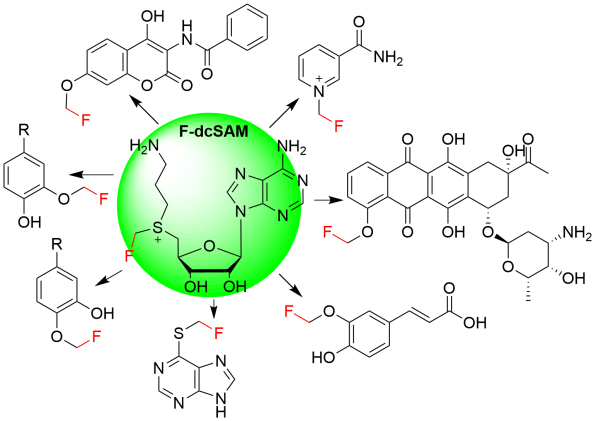
氟原子存在于20%的药物分子和30-40%的农药分子。氟甲基作为重要的含氟官能团,是生物体内很多基团电子等排体。已有多个含氟甲基药物分子和抑制剂用于临床(图1)。SAM是广泛存在于生命体的甲基化试剂,在SAM依赖型甲基转移酶的催化下可以将甲基特异性转移到核酸、蛋白质和代谢产物等多种底物。目前有机化学领域发展的多个氟甲基试剂有着和SAM 类似的硫鎓结构(图1)。因此,氟甲基SAM类似物 (F-SAM) 可以被开发作为一种氟甲基供体在甲基转移酶催化作用下实现高特异性氟甲基化反应(图2)。作者利用化学法设计合成了F-SAM。稳定性实验表明F-SAM在pH 1.0的酸性条件下具有一定的稳定性,而在pH 8.0条件下(多种甲基转移酶反应所使用的条件)在1小时内几乎完全分解。虽然有研究表明F-SAM可以通过酶法原位产生并用于转移氟甲基的级联反应,然而这种F-SAM的不稳定性限制了其成为通用的生物氟甲基化试剂。
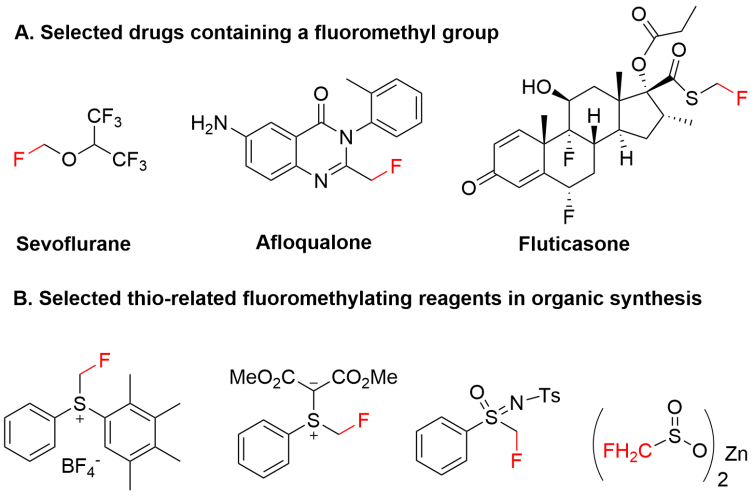
图1. 含氟甲基药物和用于有机合成的氟甲基化试剂。图片来源:ACS Catal.
SAM的结构使其容易发生羧基对Cγ,Met的分子内攻击,分解产生5’-甲硫腺苷 (MTA) 和L-高丝氨酸内酯 (HSL)。由于CH2F的诱导效应,加剧了F-SAM的分解。这与作者检测到的F-SAM分解产物一致。他们推断,不含羧基的F-SAM类似物可以通过阻止生成HSL来提高稳定性。因此,实验利用化学法设计合成了氟甲基脱羧SAM类似物:F-dcSAM。稳定性测试表明F-dcSAM的稳定性远大于F-SAM。在生理条件,F-dcSAM的半衰期超过24小时,是F-SAM的70倍。
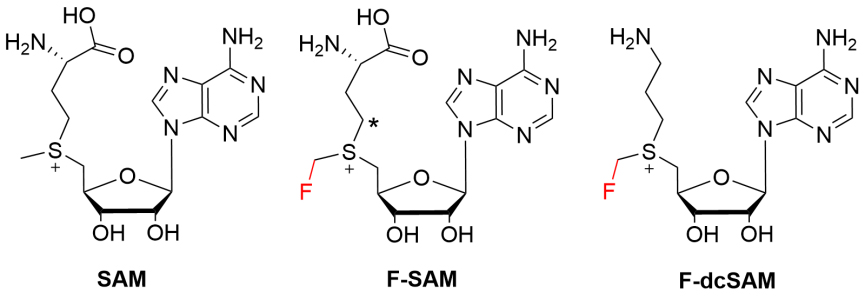
图2. SAM、F-SAM和F-dcSAM的化学结构。*表示F-SAM的Cγ,Met。图片来源:ACS Catal.
接下来,作者测试了甲基转移酶对F-dcSAM识别。首先测试了O-甲基转移酶COMT、NtCOMT和DnrK对F-dcSAM的活性。结果表明,三者均可以很好的识别F-dcSAM,并将CH2F从F-dcSAM转移到相应受体底物中。其中COMT可以将CH2F转移到多个儿茶酚类底物中,生成3-或4-氟甲氧基的产物混合物(图3)。NtCOMT可以高选择性地将氟甲基转移到咖啡酸的3-OH上,生成氟代阿魏酸(图4)。阿魏酸是许多药物分子的前体,因此,这些药物分子的氟代衍生物也可以利用氟代阿魏酸制备得到。洋红霉素及其甲基化产物柔红霉素都是抗肿瘤药物。DnrK能够催化F-dcSAM高效转移氟甲基到洋红霉素并生产氟代柔红霉素(图4)。据报道,Dnrk还可以接受其它蒽环类药物作为底物,因此这些药物分子的氟甲基类似物有望通过F-dcSAM很容易地获得。
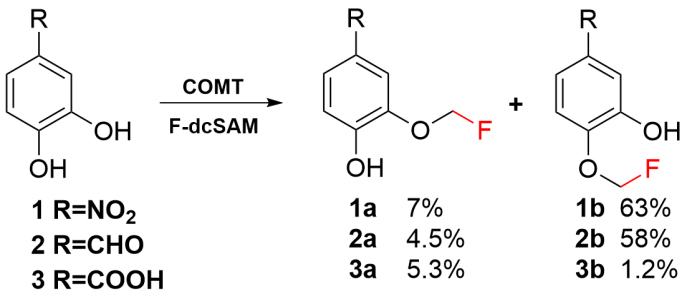
图3. COMT与F-dcSAM对不同底物的氟甲基化活性。图片来源:ACS Catal.
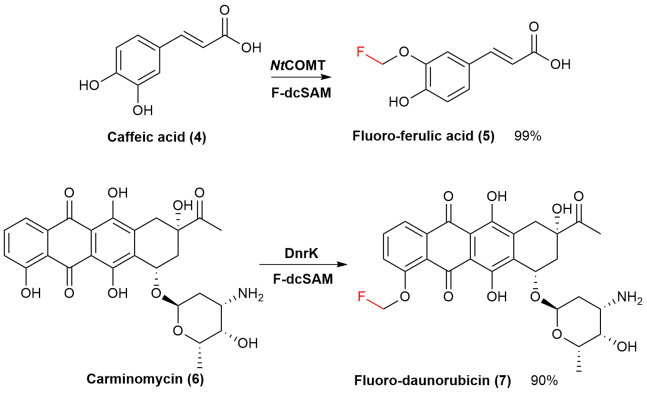
图4. F-dcSAM对天然产物咖啡酸和洋红霉素进行区域选择性氟甲基化。图片来源:ACS Catal.
接着,作者测试了C-甲基转移酶对F-dcSAM的活性。NovO是一种参与新生霉素A1生物合成的C-甲基转移酶,其催化4,7-二羟基香豆素的C-8甲基化(图5)。在NovO与F-dcSAM反应中,通过对产物分析发现,氟甲基被转移到底物的7-OH而非8-C。这种F-dcSAM引起的C/O区域选择性的转变可能由于SAM的羧基与NovO Arg116残基之间相互作用的缺失引起。
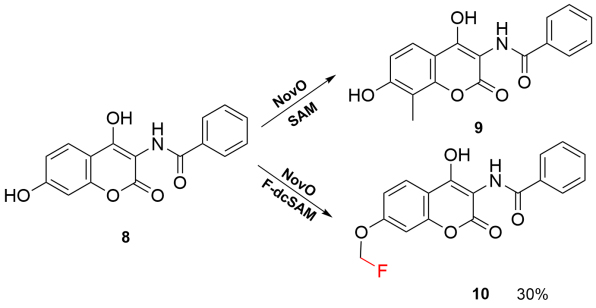
图5. NovO与SAM和F-dcSAM的反应。图片来源:ACS Catal.
S-甲基转移酶TPMT对F-dcSAM的活性测试表明,TPMT能有效地转移氟甲基从F-dcSAM到巯基嘌呤,生成6-氟甲基巯基嘌呤(图6)。由于TPMT具有较强的底物宽泛性,未来还可以利用F-dcSAM实现更多芳基硫醇的氟甲基化。
NNMT是烟酰胺N-甲基转移酶。作者研究了NNMT对F-dcSAM的活性(图6)。稳定性测试表明,仅在反应开始时形成了少量N-氟甲基烟酰胺,随着反应时间的延长,N-氟甲基烟酰胺在pH 8.0的反应体系中快速降解为起始原料。

图6. 甲基转移酶TPMT和NNMT与F-dcSAM的S-和N-氟甲基化反应。图片来源:ACS Catal.
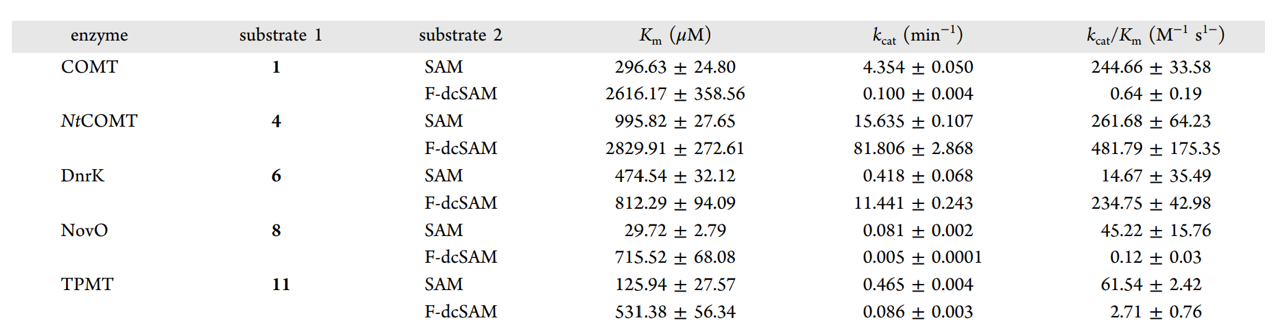
作者进一步研究了多种甲基转移酶对SAM和F-dcSAM的催化效率(表1)。动力学数据表明,由于F-dcSAM缺乏羧基,虽然与SAM相比,所有甲基转移酶与F-dcSAM表现出弱的结合力即更大的Km值。然而,NtCOMT和DnrK的kcat值F-dcSAM高于SAM,这表明由于氟甲基的原因,F-dcSAM的反应速度比SAM更快。其中,Dnrk在F-dcSAM中的kcat值是SAM的27倍,kcat/Km值是SAM的15倍,证明F-dcSAM是DnrK更好的底物。
表1. 甲基转移酶对SAM和F-dcSAM的催化效率。表格来源:ACS Catal.
除了利用化学合成制备F-dcSAM外,实验发现HMT也可以催化dcSAH和CH2FI高效合成F-dcSAM。使用HMT和甲基转移酶进行了氟甲基化的环酶级联反应,大多数甲基转移酶可实现良好的周转数。
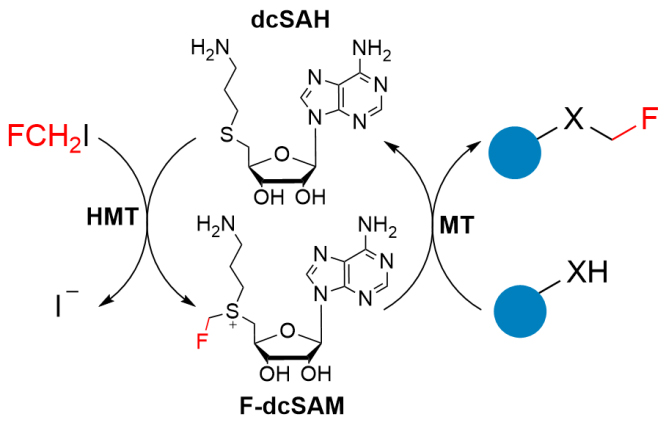
图7. 甲基转移酶 (MT)和HMT通过原位生成F-dcSAM的环酶级联反应。图片来源:ACS Catal.
综上,本研究开发了一种稳定型生物氟甲基化试剂F-dcSAM,其可以很容易地通过化学和酶法制备得到。同时,F-dcSAM还可以被多种O-、N-和S-甲基转移酶识别,通过高度区域选择性的酶促氟甲基化反应制备多种生物活性分子的氟甲基类似物,成功地将许多甲基转移酶转化为氟甲基转移酶。此外,HMT和甲基转移酶原位生成F-dcSAM的酶级联反应可实现氟甲基从CH2FI到底物的高效转移。未来通过进一步的蛋白质工程,F-dcSAM应用可以扩展到更多的甲基转移酶。因此,F-dcSAM可作为一种通用且有效的酶促氟甲基化试剂。F-dcSAM的应用为氟甲基化反应提供了一种新工具,并促进了药物分子氟类似物的制备。F-dcSAM也是第一个非芳环取代的硫鎓氟甲基试剂,为未来开发更多用于化学和生物催化的新型氟甲基化试剂提供了新思路。
这一成果近期发表在美国化学会ACS Catalysis 上。论文的第一作者为天津大学硕士生王文瑞,论文的通讯作者天津大学董敏教授。天津大学博士研究生赵慧敏、余南海和陈帆也参与了部分研究工作。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Stable S-Adenosylmethionine Analogue for Enzymatic Fluoromethylation
Wenrui Wang, Huimin Zhao, Nanhai Yu, Fan Chen, and Min Dong*
ACS Catal., 2023, 13, 13729-13734, DOI:10.1021/acscatal.3c03313
通讯作者简介
董敏,天津大学化工学院教授/博导,从事活性天然产物、蛋白质翻译后修饰的生物合成研究,特别是金属酶的功能和催化机制解析,以及酶促非天然反应的研究。课题组招聘博士后待遇从优。欢迎具有生物合成、生物催化、有机合成、药物化学等专业背景博士加盟。有意者请将个人简历发送至mindong@tju.edu.cn.
详情请见实验室主页
http://chemeng.tju.edu.cn/cn/szdw?type=detail&id=488
董敏
https://www.x-mol.com/university/faculty/64301
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
-
两个自由基SAM酶共同催化重建氧杂环丁烷核苷类抗病毒天然产物albucidin的体外合成 2022-09-17
-
甲基化试剂SAM的“菠菜” 2017-10-03
-
S-腺苷甲硫氨酸自由基酶NosL的催化多样性 2015-08-24
-
Sustainable and Scalable Enzymatic Production, Structural Elucidation, And Biological Evaluation of Novel Phlorizin AnaloguesLaurène Minsat, Yueying Li, Cédric Peyrot, Agathe Martinez, Nicolas Borie, Aurélien Peru, Blandine Godon, Clément Nève, Fanny Brunissen, Fanny Brunois, Abdouramane Dosso, Florent Allais, Jean-Hugues Renault
-
Chemical synthesis and enzymatic late-stage diversification of novel pantothenate analogues with antiplasmodial activityEuropean Journal of Medicinal Chemistry (IF 6.0) Pub Date : 2024-09-26 ,DOI:10.1016/j.ejmech.2024.116902Xiangning Liu, Sian Thistlethwaite, Rohit Kholiya, Jacob Pierscianowski, Kevin J. Saliba, Karine Auclair


































 京公网安备 11010802027423号
京公网安备 11010802027423号