赵惠民团队Nature:可见光,照亮酶催化不对称合成的新征程
副标题:光酶催化对映选择性分子间自由基氢烷基化反应
大家都知道,生命体内也时时刻刻发生着化学反应,我们的呼吸、运动、消化、生长都离不开这些反应。与实验室试管烧瓶中的化学反应不同,生命体内的化学反应多由酶催化,酶作为生物催化剂促进化学转化,具有环境友好、催化剂负载量低、选择性高、可持续性、条件温和、可进化性等特点。因此,酶催化在科学研究和工业生产上都有着广泛的应用。不过,天然酶也存在容易失活、底物范围窄等问题。为了解决这类问题,以美国加州理工学院(Caltech)的Frances H. Arnold教授为代表的科学家提出了“酶的定向进化”策略,Arnold教授还因此获得2018年诺贝尔化学奖。通过定向进化所得的酶有着科学家所希望的性质,在生物燃料、药品等等生产中有巨大的应用潜能。例如,基于进化的转氨酶的西格列汀绿色合成工艺,就曾在2010年获得“美国总统绿色化学挑战奖(Presidential Green Chemistry Challenge Award)”[1]。
此外,还有不少科学家尝试拓展酶的反应性,也就是说,让酶来催化自然界中没有催化过的反应。然而,不同于化学催化,酶催化的反应类型研究较少,如烯烃的自由基氢烷基化反应就尚未涉及。但是该反应可构筑C(sp3)-C(sp3)键,因此广泛用于制备含有α/β/γ-手性中心的羰基化合物,其中有不少γ-手性羰基化合物具有生物活性(如(+)-3-oxoabolene、(R)-1-hydroxyboivinianin A、piperidinones和(R)-4-methoxyalkanoic acids)。理论上,γ-手性羰基化合物可以通过羰基α-卤代物与非活化烯烃在光作用下发生分子间自由基氢烷基化反应得到,但该反应即使对于酶催化来说也极具挑战,原因有四:(一)产生的亲电自由基中间体需要有足够长的寿命以保证其选择性地发生交叉偶联反应而不是脱卤;(二)这种双分子转化要求羰基化合物和烯烃都要结合在酶催化中心并相互靠近;(三)新生成的C(sp3)-C(sp3)键可自由旋转且两个前手性的自由基中间体具有高度的柔性,以至于很难控制立体化学;(四)目前可见光诱导的酶催化的不对称反应还只局限于单分子转化,如不对称脱溴/脱乙酰氧基、异构化、还原、分子内自由基环化和脱羧动力学拆分,而分子间的反应还没有被报道过。
近日,美国伊利诺伊大学厄巴纳-香槟分校(UIUC)赵惠民教授(点击查看介绍)团队拓展了烯还原酶(ene-reductase, ER)的反应性。在可见光诱导下,他们利用ER将简单易得的羰基α-卤代物和末端烯烃通过不对称的分子间自由基氢烷基化反应转化为γ-手性羰基化合物(产率高达99%,ee值高达99%)。相关结果发表在Nature 上,第一作者为Xiaoqiang Huang博士。

催化不对称自由基氢烷基化构筑C(sp3)-C(sp3)键。图片来源:Nature
在自然界中,ER可以催化羰基取代的烯烃发生2-电子还原,其催化中心上的组氨酸和天冬氨酸残基(有时是两个组氨酸)可以结合羰基,GDH/NADP+/葡萄糖基辅因子再生系统原位形成的黄素单核苷酸对苯二酚阴离子(FMNH-)可以提供氢源,酪氨酸残基可以作为质子供体。研究者猜想,ER的这些特征或许有利于分子间的不对称氢烷基化反应。
为了验证猜想,研究人员选择α-溴代苯乙酮(1a)和α-甲基苯乙烯(1b)作为底物,在三羟甲基氨基甲烷缓冲液(Tris buffer,pH 7.6)和厌氧条件及蓝光照射下进行ER酶的筛选。结果显示,由恶臭假单胞菌(Pseudomonas putida)产生的两种ER酶XenA和XenB都能以中等的立体选择性得到R-3a(ee值均为49%)。由伯氏耶尔森菌(Yersinia bercovieri)产生的YersER可以64%的ee值得到S-3a。由酿酒酵母(Saccharomyces cerevisiae)产生的OYE1则能以 94%的ee值得到S-3a(尽管收率仅为21%);随后通过加入甘油和DMSO作为助溶剂,同时将催化剂负载量增加到1 mol%,S-3a的收率和ee值分别提高到88%和96%。对照实验结果证明,ER酶、可见光、辅因子再生系统对于反应都是必不可少(下图b,entries 1-4)。
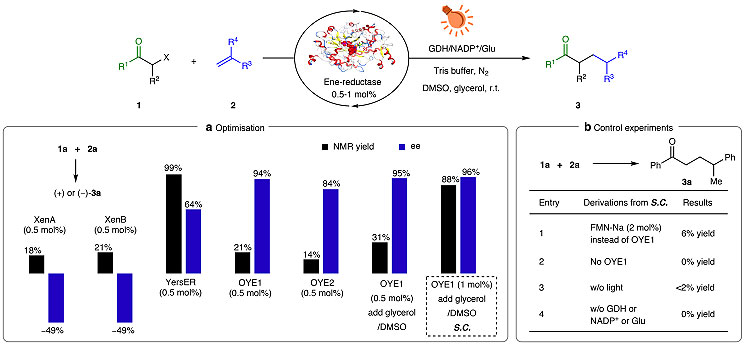
ER酶筛选及对照实验。图片来源:Nature
接着,研究人员进行了底物扩展。α-溴代芳基酮上取代基的位置和电性对反应的影响不大,都能以74–99%的收率和93–98%的ee值得到具有γ-立体中心的酮(3a-3h)。α-溴代酰胺(1i)以及对小分子氢键催化剂无效的α-溴代1,3-二酯(1k)和α-溴代酯(1j、1m)也能兼容该反应,只是酶需要改变一下(酰胺用YersER,酯用XenA);二级α-溴代羰基化合物(1l、1m)也能给出很好的ee值(up to 99%),只是非对映选择性一般。此外,不同的α-甲基芳基取代的乙烯也能兼容该反应(3n-3p,收率:58–83%,ee值:97–98%);烯炔(3q)和α-乙基苯乙烯(3r)的反应效果则有所下降;而脂肪族烯烃或非末端烯烃虽也能反应,但反应的对映选择性很差。
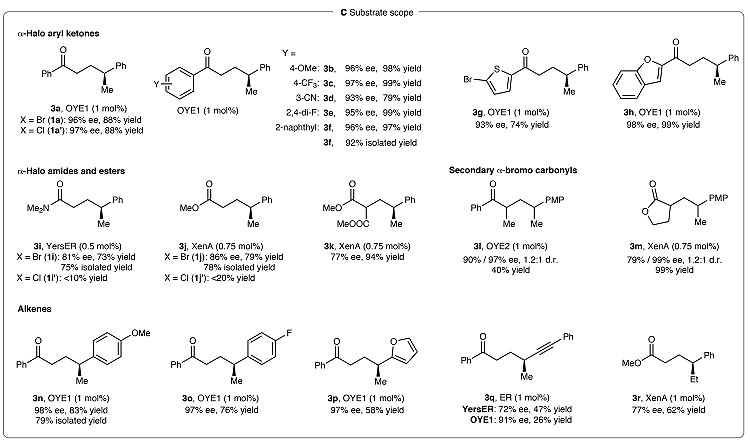
底物扩展研究。图片来源:Nature
他们设想的催化循环如下图所示:起初,GDH将NADP+还原为NADPH,后者将氢化物转移到ER并产生FMNH-。然后,α-卤代羰基化合物通过与上述His/Asn残基形成的氢键相互作用结合在酶的活性位点上,与相邻的FMNH-形成电子供体-受体复合物(EDA complex,Int. B)。接着,EDA被可见光激发,通过单电子转移脱卤转化为Int. C,其中包含两个自由基:α-羰基碳中心自由基和FMNH•。随后Int. C与前手性烯烃发生自由基加成得到Int. D,后者通过立体控制的氢原子转移(HAT)得到Int. E。最后,发生产物/底物交换以及GDH/NADP+/葡萄糖体系对FMNH-的再生完成了催化循环。
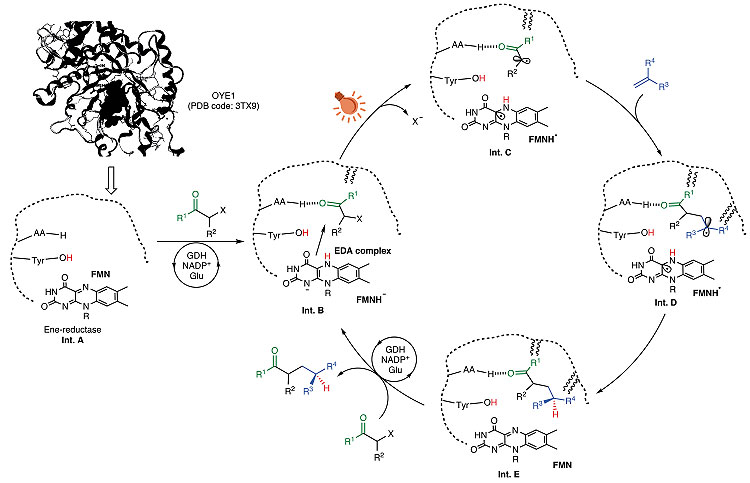
假设的催化循环。图片来源:Nature
为了验证设想的机理,研究人员进行了一系列实验。首先,UV-Vis吸收光谱证实了EDA复合物(Int. B)的存在(下图a),因为含有FMN的YersER在可见光区有很强的吸收带;加入GDH/NADP+/葡萄糖后体系变成无色,这表明醌式的FMN被还原成FMNH-;当再加入羰基底物时,在蓝光区域出现明显的吸收带,这表明了EDA复合物的形成。接着,通过自由基钟实验证明了Int. D的存在(下图b),因为使用α-环丙基苯乙烯时,主要检测到开环产物5。然后,通过氘标记实验证明了氢转移过程(Int. D→Int. E,下图c),因为在1a + 2a→3a的反应中使用FMND-(由D-葡萄糖-1,2,3,4,5,6,6-d7原位生成)会得到49%氘代的产物;如果再加入氘代缓冲溶液,产物的氘代率可提高至83%,这说明氢转移过程中氢原子主要来自于FMNH•,少部分来自溶剂或氨基酸残基上的活泼氢。
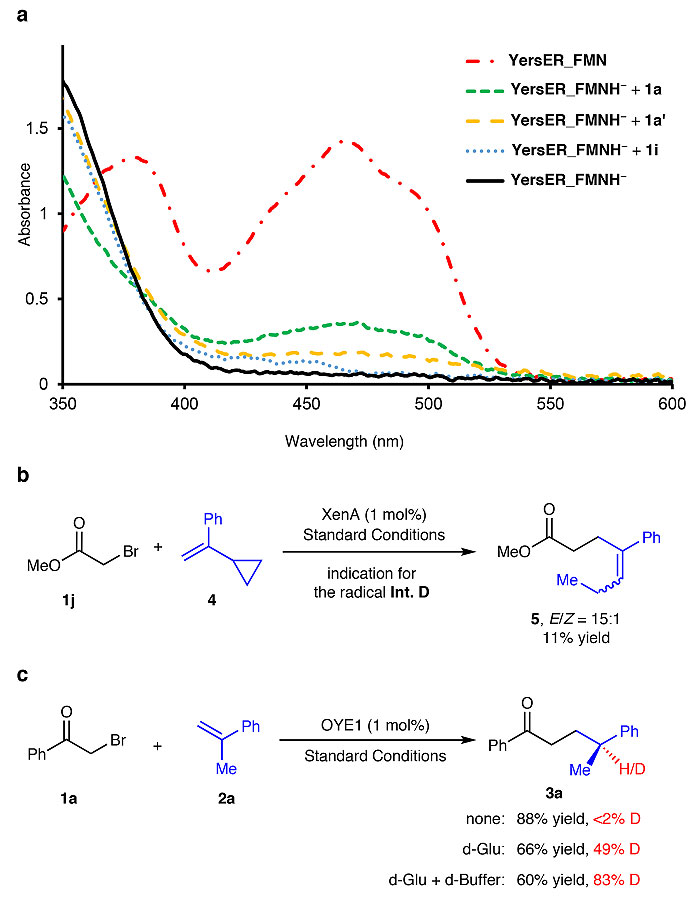
机理验证实验。图片来源:Nature
另外,研究人员还通过多尺度模拟进行了理论验证,包括经典的分子动力学(MD)模拟、QM/MM(量子力学/分子力学)-MD模拟和DFT计算,这些结果支持在含Cl-的缓冲溶液中Br/Cl交换是有利的。接着,对1a' + 2a→3a进行模拟,QM/MM-MD平衡的EDA复合物表明1a'通过与FMNH-和Phe250形成π–π堆积以及与Asn194形成氢键锚定在EDA中。基于QM/MM的自由能计算结果显示无可见光时,基态EDA复合物不能产生α-酮自由基,而通过非自由基过程反应则需要越过很高的能垒,这也与实验结果一致(3a的生成需要可见光)。同时,含时密度泛函理论(TDDFT)和电荷密度差计算也显示第一单线态激发态(S1)涉及到Int. B 中FMNH-的π轨道向1a'的π* 轨道的电荷转移,并处于可见光范围内。在S1下,C−Cl键切断形成FMNH•和苯甲酰基自由基几乎是无障碍的(Int. B → Int. C,下图d),然后苯甲酰基自由基被烯烃2a捕获,该过程的吉布斯自由能能垒仅2.6 kcal/mol(Int. C → Int. D,下图e)。相比之下,直接从FMNH•到苯甲酰基自由基的HAT过程导致脱卤化是不利的(ΔG≠ = 4.4 kcal/mol)。这些理论计算都表明双分子的自由基交叉偶联要比脱卤在能量上更有利,这就是该反应化学选择性的依据。
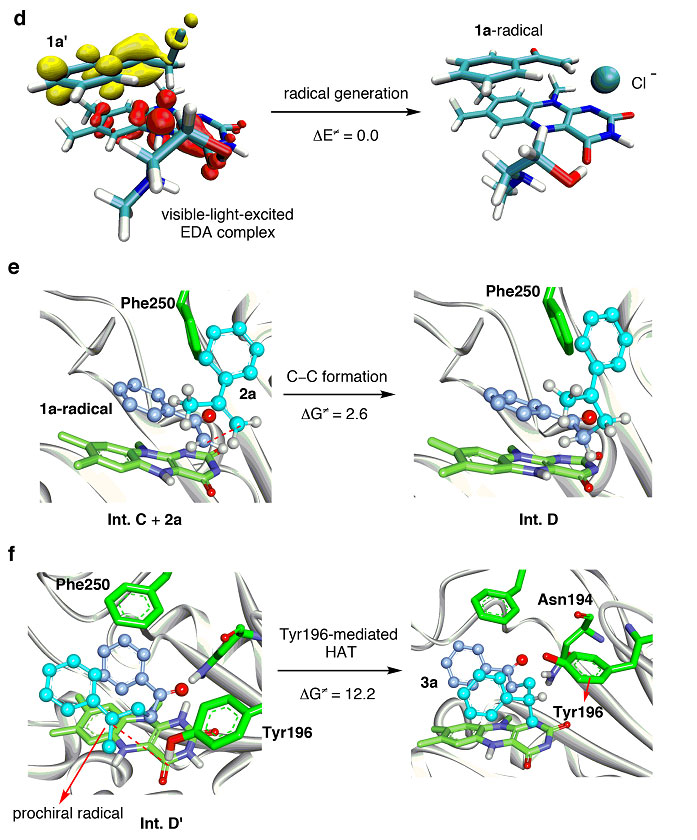
机理验证。图片来源:Nature
另一个关键问题就是如何解释立体化学的起源,主要涉及氢转移过程(Int. D → Int. E)。如上图f中QM/MM-MD平衡的活性位点结构所示,前手性自由基(Int. D')夹在FMNH•和Phe250之间,且后者与Asn194形成氢键,Int. D'苄位自由基位点靠近Tyr196的活泼氢,而FMNH•上的氢原子则离的比较远。基于QM/MM的自由能计算显示,从Tyr196发生氢转移(ΔG≠ =12.2 kcal/mol)形成S-3a要比从FMNH•进行氢转移更有利,因为后者存在较大的位阻排斥和较长的距离(形成R-3a)。然后,生成的Tyr196自由基从FMNH•攫取氢原子恢复静息态的ER(ΔG≠ = 18.6 kcal/mol)。这些计算结果与氘代实验一致,揭示了一种Tyr196介导的氢转移过程。
总结
赵惠民教授团队突破了ER原本反应性的限制,通过引入光催化将功能延伸到分子间的不对称自由基氢烷基化反应。这一成果对于开发出高效光酶催化反应有重要的启示,科学家们或许能够更多地拓展酶的反应性,或者将几种酶结合起来,探索新的反应性选择。
原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Photoenzymatic enantioselective intermolecular radical hydroalkylation
Xiaoqiang Huang, Binju Wang, Yajie Wang, Guangde Jiang, Jianqiang Feng, Huimin Zhao
Nature, 2020, DOI: 10.1038/s41586-020-2406-6
导师介绍
赵惠民
https://www.x-mol.com/university/faculty/66044
参考资料:
1. Presidential Green Chemistry Challenge: 2010 Greener Reaction Conditions Award
(本文由峰千朵供稿)
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
-
西南大学:酶和光接力催化实现吲哚的氨烷基化反应 2016-10-28
-
容器不同,产物也不同:首例二甲胺参与的烯烃氢氨烷基化反应 2017-12-11
-
光和酶协作催化的不对称反应 2019-02-12


































 京公网安备 11010802027423号
京公网安备 11010802027423号