张庆伟/朱棣等JMC封面:新型β-catenin/BCL9小分子 PPI抑制剂单独或联合PD-1用于结直肠癌靶向治疗
目前,世界范围内结直肠癌患者确诊人数位居第三位,且致死率高。结直肠癌的主要治疗手段包括手术和化疗,但60-70%患者在被诊断时癌细胞已发生转移,导致不良预后或无法通过手术完全切除,化疗仍然是治疗结直肠癌的主要方式。然而,化疗存在毒性大和耐药问题,目前免疫疗法对90%结直肠癌患者响应率低。因此,亟需新型靶向药物或者药物组合策略用于结直肠癌治疗。
研究发现,约80%的结直肠癌中Wnt/β-catenin信号异常激活,且异常激活的Wnt/β-catenin信号通路与免疫逃逸密切相关。β-catenin/BCL9蛋白-蛋白相互作用是Wnt/β-catenin信号激活的最后一步,BCL9在结肠癌中也是高表达,敲除BCL9可显著抑制结直肠癌的生长且显示免疫增效作用。综上,抑制β-catenin/BCL9相互作用阻断Wnt/β-catenin信号理论上可达到抑制结直肠癌的生长,调节肿瘤微环境增强PD-1药效的目的。
近日,中国医药工业研究总院张庆伟/李建其教授团队和复旦大学基础医学院朱棣教授团队以具有一定成药性的苯基哌啶骨架为先导,通过分子对接,确定化合物与蛋白结合模式,并通过三轮先导物结构优化,最终发现化合物41体外蛋白(IC50 = 0.72μM)及细胞(IC50 = 0.66μM)活性最优,相较于先导化合物活性分别提升7倍和18倍。
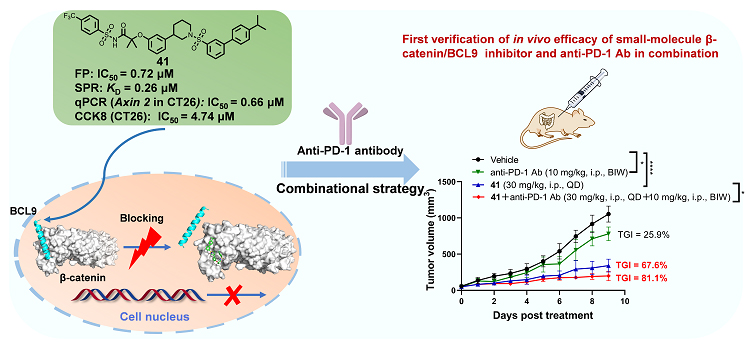
图1. 文章图片摘要
随后,细胞实验显示化合物41具有低细胞毒性,可选择性抑制Wnt-依赖的结直肠癌细胞的生长,在高浓度下不会对Wnt-非依赖的细胞产生抑制作用,对结肠癌细胞CT26抑制活性最优(IC50 = 4.74 μM),优于阳性对照ICG-001。此外,化合物41可促进Wnt-依赖的结直肠癌细胞的凋亡,呈浓度依赖的抑制CT26细胞的迁移。在CT26细胞中,41可通过抑制Wnt靶基因Axin2、Ccnd1、Cd44和Vegfa的表达,下调Axin2和Cyclin D1蛋白水平。
初步成药性研究发现,化合物41在人、小鼠和大鼠中肝微粒体代谢稳定。在CT26肿瘤体内模型中,化合物41可浓度依赖的抑制肿瘤的生长,30 mg/kg的给药剂量下,抑瘤率为67.6%,显著优于阳性对照药ICG-001。并且,与PD-1抗体联用后,体内抑瘤率提升至81.1%,显著优于化合物41或PD-1抗体单独给药,证明化合物41与PD-1抗体用于结直肠癌治疗具有体内协同作用。
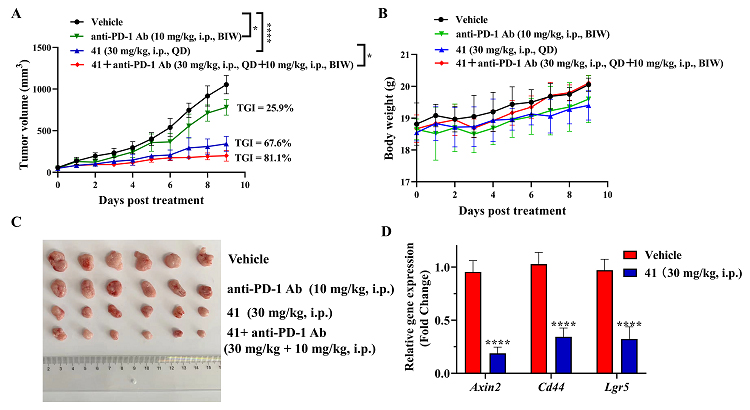
图2. 化合物41体内实验结果
以上研究成果被杂志编辑推荐作为封面文章发表在药物化学专业国际顶级期刊Journal of Medicinal Chemistry 上。复旦大学和中国医药工业研究总院联培博士生张浩为第一作者,复旦大学博士生刘成龙为共同第一作者,中国医药工业研究总院张庆伟研究员、李建其研究员和复旦大学朱棣教授、王永辉教授为共同通讯作者。在本文发表之前,团队应杂志编辑邀请已在Journal of Medicinal Chemistry 发表综述文章一篇,对β-catenin/BCL9 PPI抑制剂领域最新研究进展做了全面系统的分析和总结(J. Med. Chem., 2023, 66, 1-31,点击阅读详细)。

原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):

Discovery of Novel 3-Phenylpiperidine Derivatives Targeting the β-Catenin/B-Cell Lymphoma 9 Interaction as a Single Agent and in Combination with the Anti-PD-1 Antibody for the Treatment of Colorectal Cancer
Hao Zhang, Chenglong Liu, Qiushi Chen, Li-An Shen, Wenting Xiao, Jiayi Li, Yonghui Wang*, Di Zhu*, Qingwei Zhang*, and Jianqi Li*
J. Med. Chem., 2023, 66, 1349–1379, DOI: 10.1021/acs.jmedchem.2c01568
研究团队简介

张庆伟,中国医药工业研究总院研究员,院一级学科带头人,博士生导师,科技部国家科技专家库专家,上海市药学会药物化学专业委员会委员,上海市科技专家库专家,上海技术交易所专家智库专家。主要研究领域:1)中枢神经系统、靶向肿瘤免疫及心脑血管等原创性新药设计、合成及成药性评价;2)药物关键中间体的高效合成方法学研究及具有药用价值天然活性单体全合成研究;3)重大医药品种的绿色工艺产业化开发研究。以第一或通讯作者在Journal of Medicinal Chemistry,European Journal of Medicinal Chemistry, Bioorganic Chemistry,Bioorganic & Medicinal Chemistry Letters ,Chinese Chemical Letters,Bioorganic & Medicinal Chemistry等SCI期刊上发表研究论文40余篇,其中中科院一区Top期刊论文10余篇;获中国发明专利授权近30项,美国专利授权2项,欧洲专利授权1项;参与撰写2本英文专业书籍;主持国家十三.五“重大新药创制”科技重大专项、国家自然基金项目、上海市“科技创新行动计划”等项目9项,发现6个高效低毒、具有自主知识产权及综合竞争优势的候选新药,其中4个候选新药已成功转让企业;主持完成1类新药安喹利司原料药等10余个医药品种的产业化开发及申报。个人先后获得上海市 “青年科技英才”、 上海市静安区 “静安青年英才”、上海市青年五四奖章(个人)、上海市“青年科技启明星”、 “国药集团青年榜样”、共青团中央“全国向上向善好青年”候选人等荣誉称号。

朱棣,复旦大学基础医学院博士生导师,复旦卓识人才。2015年受聘为哈佛大学医学院医学讲师(junior faculty)。主要研究领域、方向:1. 肿瘤免疫药理学机制研究;2. 肿瘤靶向治疗新药开发。第一或通讯代表作发表在 Nature Medicine, Cancer Discovery, Science Translational Medicine , Science Advances, Signal Transduction and Targeted Therapy, Cell Reports,Pharmacological Research等杂志。总共发表SCI论文30篇,总影响因子426分。主持项目14项。专利授权4项。开发多项创新肿瘤免疫疗法,2项成果已经进入非注册临床试验。1项新药研发成果完成企业转化。受邀在2017年美国AACR年会分论坛做大会报告。中国药理学会化药专业委员会专业委员,上海市生物工程学会细胞治疗专委会专业委员。研究成果获得Nature Reviews Clinical Oncology, Cancer Discovery专栏报道,以及新民网、文汇报等媒体报道。获得上海市生物工程学会“东富龙”生物工程优秀青年科学家等荣誉称号。
https://www.x-mol.com/university/faculty/62853

李建其,理学博士,研究员,博士生导师,曾任上海医药工业研究院化学制药新技术中心主任,上海市药化专委会副主任委员,上海药物合成工艺过程工程技术研究中心主任。主要进行中枢神经系统、非细胞毒类抗肿瘤等原创性新药研究及药品的产业化开发。曾获得国家科技进步三等奖、国务院政府专家特殊津贴、上海市首届优秀留学归国人员浦江计划资助及中央企业劳动模范称号。其研究团队在抗脑中风、抗抑郁症、抗精神分裂、中枢镇痛及抗肿瘤研究领域各有候选药物处于临床前系统研究阶段。完成60 多个药品的合成新技术和产业化研究,20 多个品种获得相应临床批件和生产批件。承担多项国家科委和上海市科委重大科研项目。
如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载!
-
J Med Chem:β‑Catenin与其核内蛋白相互作用抑制剂的药物化学研发策略 2023-01-16
-
独脚金内酯衍生物作为新型抑制剂及其在结直肠癌治疗中的应用 2022-07-30
-
Discovery of Novel 3-Phenylpiperidine Derivatives Targeting the β-Catenin/B-Cell Lymphoma 9 Interaction as a Single Agent and in Combination with the Anti-PD-1 Antibody for the Treatment of Colorectal CancerHao Zhang, Chenglong Liu, Qiushi Chen, Li-An Shen, Wenting Xiao, Jiayi Li, Yonghui Wang, Di Zhu, Qingwei Zhang, Jianqi Li
-
Design, synthesis and biological evaluation of quercetin derivatives as novel β-catenin/B-cell lymphoma 9 protein−protein interaction inhibitorsEuropean Journal of Medicinal Chemistry (IF 6.0) Pub Date : 2022-12-31 ,DOI:10.1016/j.ejmech.2022.115075Li-An Shen, Xinyan Peng, Ya Bao, Chenglong Liu, Hao Zhang, Jianqi Li, Di Zhu, Qingwei Zhang
-
Discovery of Novel Allosteric EGFR L858R Inhibitors for the Treatment of Non-Small-Cell Lung Cancer as a Single Agent or in Combination with OsimertinibUlrike Obst-Sander, Antonio Ricci, Bernd Kuhn, Thomas Friess, Philipp Koldewey, Andreas Kuglstatter, David Hewings, Annick Goergler, Sandra Steiner, Daniel Rueher, Marie-Paule Imhoff, Noemi Raschetti, Hans-Peter Marty, Aline Dietzig, Caroline Rynn, Andreas Ehler, Dominique Burger, Martin Kornacker, Jeannine Petrig Schaffland, Frank Herting, William Pao, James R. Bischoff, Bruno Martoglio, Yvonne Alice Nagel, Georg Jaeschke
-
Systems Drug Discovery for Diffuse Large B Cell Lymphoma Based on Pathogenic Molecular Mechanism via Big Data Mining and Deep Learning MethodInternational Journal of Molecular Sciences (IF 4.9) Pub Date : 2022-06-16 ,DOI:10.3390/ijms23126732Shan-Ju Yeh, Tsun-Yung Yeh, Bor-Sen Chen
-
Single-cell profiling reveals the importance of CXCL13/CXCR5 axis biology in lymphocyte-rich classic Hodgkin lymphoma [Immunology and Inflammation]Proceedings of the National Academy of Sciences of the United States of America (IF 9.4) Pub Date : 2021-10-12 ,DOI:10.1073/pnas.2105822118Tomohiro Aoki, Lauren C. Chong, Katsuyoshi Takata, Katy Milne, Ashley Marshall, Elizabeth A. Chavez, Tomoko Miyata-Takata, Susana Ben-Neriah, Doria Unrau, Adele Telenius, Merrill Boyle, Andrew P. Weng, Kerry J. Savage, David W. Scott, Pedro Farinha, Sohrab P. Shah, Brad H. Nelson, Christian Steidl


































 京公网安备 11010802027423号
京公网安备 11010802027423号