当前位置:
X-MOL 学术
›
Angew. Chem. Int. Ed.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Enantioselective Aminohydroxylation of Styrenyl Olefins Catalyzed by an Engineered Hemoprotein.
Angewandte Chemie International Edition ( IF 16.1 ) Pub Date : 2019-01-25 , DOI: 10.1002/anie.201812968 Inha Cho 1 , Christopher K Prier 1, 2 , Zhi-Jun Jia 1 , Ruijie K Zhang 1 , Tamás Görbe 1, 3 , Frances H Arnold 1
Angewandte Chemie International Edition ( IF 16.1 ) Pub Date : 2019-01-25 , DOI: 10.1002/anie.201812968 Inha Cho 1 , Christopher K Prier 1, 2 , Zhi-Jun Jia 1 , Ruijie K Zhang 1 , Tamás Görbe 1, 3 , Frances H Arnold 1
Affiliation
|
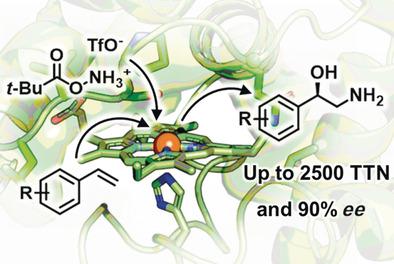
Chiral 1,2‐amino alcohols are widely represented in biologically active compounds from neurotransmitters to antivirals. While many synthetic methods have been developed for accessing amino alcohols, the direct aminohydroxylation of alkenes to unprotected, enantioenriched amino alcohols remains a challenge. Using directed evolution, we have engineered a hemoprotein biocatalyst based on a thermostable cytochrome c that directly transforms alkenes to amino alcohols with high enantioselectivity (up to 2500 TTN and 90 % ee) under anaerobic conditions with O‐pivaloylhydroxylamine as an aminating reagent. The reaction is proposed to proceed via a reactive iron‐nitrogen species generated in the enzyme active site, enabling tuning of the catalyst's activity and selectivity by protein engineering.
中文翻译:

工程血红蛋白催化苯乙烯基烯烃的对映选择性氨基羟化反应。
从神经递质到抗病毒剂的生物活性化合物中广泛存在手性1,2-氨基醇。尽管已经开发出许多用于获得氨基醇的合成方法,但是烯烃直接氨基羟基化为未保护的,对映体富集的氨基醇仍然是一个挑战。使用定向进化,我们设计了一种基于热稳定细胞色素c的血红蛋白生物催化剂,该生物色素在厌氧条件下使用O将烯烃直接以高对映选择性(高达2500 TTN和90%ee)转化为氨基醇。新戊酰羟胺作为胺化剂。建议该反应通过在酶活性位点产生的反应性铁氮物种进行,从而可以通过蛋白质工程调节催化剂的活性和选择性。
更新日期:2019-01-25
中文翻译:

工程血红蛋白催化苯乙烯基烯烃的对映选择性氨基羟化反应。
从神经递质到抗病毒剂的生物活性化合物中广泛存在手性1,2-氨基醇。尽管已经开发出许多用于获得氨基醇的合成方法,但是烯烃直接氨基羟基化为未保护的,对映体富集的氨基醇仍然是一个挑战。使用定向进化,我们设计了一种基于热稳定细胞色素c的血红蛋白生物催化剂,该生物色素在厌氧条件下使用O将烯烃直接以高对映选择性(高达2500 TTN和90%ee)转化为氨基醇。新戊酰羟胺作为胺化剂。建议该反应通过在酶活性位点产生的反应性铁氮物种进行,从而可以通过蛋白质工程调节催化剂的活性和选择性。


















































 京公网安备 11010802027423号
京公网安备 11010802027423号