当前位置:
X-MOL 学术
›
Adv. Mater.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
A Biomimetic Non-Antibiotic Approach to Eradicate Drug-Resistant Infections.
Advanced Materials ( IF 27.4 ) Pub Date : 2018-12-27 , DOI: 10.1002/adma.201806024 Yu Zhao 1 , Qianqian Guo 1 , Xiaomei Dai 1 , Xiaosong Wei 1 , Yunjian Yu 1 , Xuelei Chen 1 , Chaoxing Li 1 , Zhiqiang Cao 2 , Xinge Zhang 1
Advanced Materials ( IF 27.4 ) Pub Date : 2018-12-27 , DOI: 10.1002/adma.201806024 Yu Zhao 1 , Qianqian Guo 1 , Xiaomei Dai 1 , Xiaosong Wei 1 , Yunjian Yu 1 , Xuelei Chen 1 , Chaoxing Li 1 , Zhiqiang Cao 2 , Xinge Zhang 1
Affiliation
|
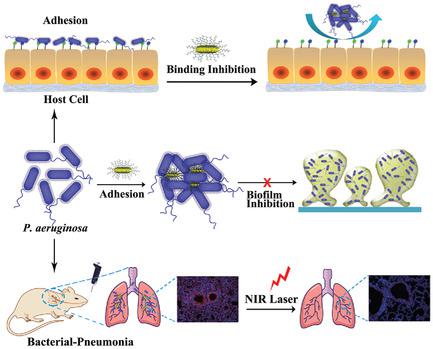
The chronic infections by pathogenic Pseudomonas aeruginosa (P. aeruginosa) remain to be properly addressed. In particular, for drug-resistant strains, limited medication is available. An in vivo pneumonia model induced by a clinically isolated aminoglycoside resistant strain of P. aeruginosa is developed. Tobramycin clinically treating P. aeruginosa infections is found to be ineffective to inhibit or eliminate this drug-resistant strain. Here, a newly developed non-antibiotics based nanoformulation plus near-infrared (NIR) photothermal treatment shows a remarkable antibacterial efficacy in treating this drug-resistant pneumonia. The novel formulation contains 50-100 nm long nanorods decorated with two types of glycomimetic polymers to specifically block bacterial LecA and LecB lectins, respectively, which are essential for bacterial biofilm development. Such a 3D display of heteromultivalent glycomimetics on a large scale is inspired by the natural strengthening mechanism for the carbohydrate-lectin interaction that occurs when bacteria initially infects the host. This novel formulation shows the most efficient bacteria inhabitation and killing against P. aeruginosa infection, through lectin blocking and the near-infrared-light-induced photothermal effect of gold nanorods, respectively. Collectively, the novel biomimetic design combined with the photothermal killing capability is expected to be an alternative treatment strategy against the ever-threatening drug-resistant infectious diseases when known antibiotics have failed.
中文翻译:

一种仿生非抗生素方法来根除抗药性感染。
致病性铜绿假单胞菌(P. aeruginosa)的慢性感染仍有待适当解决。特别是对于耐药菌株,只能使用有限的药物。建立了由临床分离的铜绿假单胞菌的氨基糖苷抗药性菌株诱导的体内肺炎模型。已发现临床上治疗铜绿假单胞菌感染的妥布霉素对抑制或消除这种耐药菌株无效。在这里,新开发的基于非抗生素的纳米制剂加近红外(NIR)光热处理在治疗这种耐药性肺炎中显示出显着的抗菌功效。新的配方包含50-100 nm长的纳米棒,上面装饰有两种类型的拟糖聚合物,分别特异性阻断细菌LecA和LecB凝集素,这对于细菌生物膜的发育至关重要。杂合多价糖模拟物的这种3D显示大规模地受到了细菌最初感染宿主时发生的碳水化合物-凝集素相互作用的天然增强机制的启发。这种新颖的配方分别通过凝集素阻滞和近红外光诱导的金纳米棒的光热作用,显示出最有效的细菌栖息和杀灭铜绿假单胞菌感染的能力。总的来说,当已知的抗生素失效时,新颖的仿生设计与光热杀伤能力的结合有望成为对抗不断威胁的耐药性传染病的另一种治疗策略。杂合多价糖模拟物的这种3D显示大规模地受到了细菌最初感染宿主时发生的碳水化合物-凝集素相互作用的天然增强机制的启发。这种新颖的配方分别通过凝集素阻滞和近红外光诱导的金纳米棒的光热作用,显示出最有效的细菌栖息和杀灭铜绿假单胞菌感染的能力。总的来说,当已知的抗生素失效时,新颖的仿生设计与光热杀伤能力的结合有望成为对抗不断威胁的耐药性传染病的另一种治疗策略。杂合多价糖模拟物的这种3D显示大规模地受到了当细菌最初感染宿主时发生的碳水化合物-凝集素相互作用的天然增强机制的启发。这种新颖的配方分别通过凝集素阻滞和近红外光诱导的金纳米棒的光热作用,显示出最有效的细菌栖息和杀灭铜绿假单胞菌感染的能力。总的来说,当已知的抗生素失效时,新颖的仿生设计与光热杀伤能力的结合有望成为对抗不断威胁的耐药性传染病的另一种治疗策略。这种新颖的配方分别通过凝集素阻滞和近红外光诱导的金纳米棒的光热作用,显示出最有效的细菌栖息和杀灭铜绿假单胞菌感染的能力。总的来说,当已知的抗生素失效时,新颖的仿生设计与光热杀伤能力的结合有望成为对抗不断威胁的耐药性传染病的另一种治疗策略。这种新颖的配方分别通过凝集素阻滞和近红外光诱导的金纳米棒的光热作用,显示出最有效的细菌栖息和杀灭铜绿假单胞菌感染的能力。总的来说,当已知的抗生素失效时,新颖的仿生设计与光热杀伤能力的结合有望成为对抗不断威胁的耐药性传染病的另一种治疗策略。
更新日期:2018-12-27
中文翻译:

一种仿生非抗生素方法来根除抗药性感染。
致病性铜绿假单胞菌(P. aeruginosa)的慢性感染仍有待适当解决。特别是对于耐药菌株,只能使用有限的药物。建立了由临床分离的铜绿假单胞菌的氨基糖苷抗药性菌株诱导的体内肺炎模型。已发现临床上治疗铜绿假单胞菌感染的妥布霉素对抑制或消除这种耐药菌株无效。在这里,新开发的基于非抗生素的纳米制剂加近红外(NIR)光热处理在治疗这种耐药性肺炎中显示出显着的抗菌功效。新的配方包含50-100 nm长的纳米棒,上面装饰有两种类型的拟糖聚合物,分别特异性阻断细菌LecA和LecB凝集素,这对于细菌生物膜的发育至关重要。杂合多价糖模拟物的这种3D显示大规模地受到了细菌最初感染宿主时发生的碳水化合物-凝集素相互作用的天然增强机制的启发。这种新颖的配方分别通过凝集素阻滞和近红外光诱导的金纳米棒的光热作用,显示出最有效的细菌栖息和杀灭铜绿假单胞菌感染的能力。总的来说,当已知的抗生素失效时,新颖的仿生设计与光热杀伤能力的结合有望成为对抗不断威胁的耐药性传染病的另一种治疗策略。杂合多价糖模拟物的这种3D显示大规模地受到了细菌最初感染宿主时发生的碳水化合物-凝集素相互作用的天然增强机制的启发。这种新颖的配方分别通过凝集素阻滞和近红外光诱导的金纳米棒的光热作用,显示出最有效的细菌栖息和杀灭铜绿假单胞菌感染的能力。总的来说,当已知的抗生素失效时,新颖的仿生设计与光热杀伤能力的结合有望成为对抗不断威胁的耐药性传染病的另一种治疗策略。杂合多价糖模拟物的这种3D显示大规模地受到了当细菌最初感染宿主时发生的碳水化合物-凝集素相互作用的天然增强机制的启发。这种新颖的配方分别通过凝集素阻滞和近红外光诱导的金纳米棒的光热作用,显示出最有效的细菌栖息和杀灭铜绿假单胞菌感染的能力。总的来说,当已知的抗生素失效时,新颖的仿生设计与光热杀伤能力的结合有望成为对抗不断威胁的耐药性传染病的另一种治疗策略。这种新颖的配方分别通过凝集素阻滞和近红外光诱导的金纳米棒的光热作用,显示出最有效的细菌栖息和杀灭铜绿假单胞菌感染的能力。总的来说,当已知的抗生素失效时,新颖的仿生设计与光热杀伤能力的结合有望成为对抗不断威胁的耐药性传染病的另一种治疗策略。这种新颖的配方分别通过凝集素阻滞和近红外光诱导的金纳米棒的光热作用,显示出最有效的细菌栖息和杀灭铜绿假单胞菌感染的能力。总的来说,当已知的抗生素失效时,新颖的仿生设计与光热杀伤能力的结合有望成为对抗不断威胁的耐药性传染病的另一种治疗策略。































 京公网安备 11010802027423号
京公网安备 11010802027423号