Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Linking a cell-division gene and a suicide gene to define and improve cell therapy safety
Nature ( IF 50.5 ) Pub Date : 2018-11-01 , DOI: 10.1038/s41586-018-0733-7 Qin Liang , Claudio Monetti , Maria V. Shutova , Eric J. Neely , Sabiha Hacibekiroglu , Huijuan Yang , Christopher Kim , Puzheng Zhang , Chengjin Li , Kristina Nagy , Maria Mileikovsky , Istvan Gyongy , Hoon-Ki Sung , Andras Nagy
Nature ( IF 50.5 ) Pub Date : 2018-11-01 , DOI: 10.1038/s41586-018-0733-7 Qin Liang , Claudio Monetti , Maria V. Shutova , Eric J. Neely , Sabiha Hacibekiroglu , Huijuan Yang , Christopher Kim , Puzheng Zhang , Chengjin Li , Kristina Nagy , Maria Mileikovsky , Istvan Gyongy , Hoon-Ki Sung , Andras Nagy
|
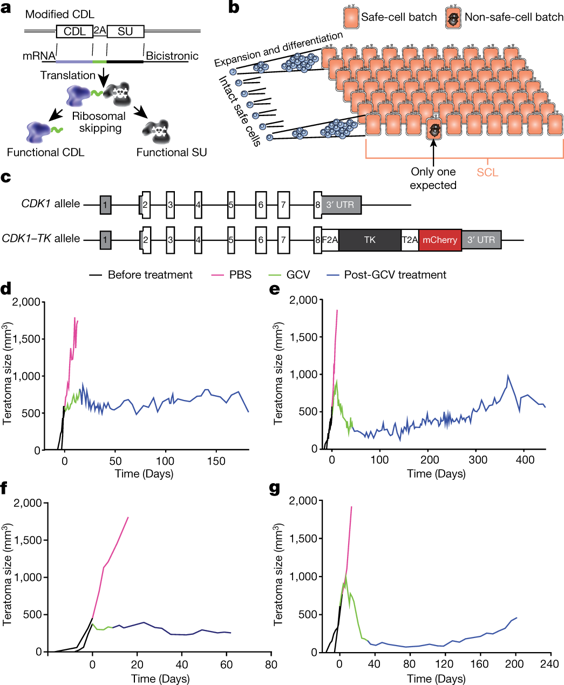
Human pluripotent cell lines hold enormous promise for the development of cell-based therapies. Safety, however, is a crucial prerequisite condition for clinical applications. Numerous groups have attempted to eliminate potentially harmful cells through the use of suicide genes1, but none has quantitatively defined the safety level of transplant therapies. Here, using genome-engineering strategies, we demonstrate the protection of a suicide system from inactivation in dividing cells. We created a transcriptional link between the suicide gene herpes simplex virus thymidine kinase (HSV-TK) and a cell-division gene (CDK1); this combination is designated the safe-cell system. Furthermore, we used a mathematical model to quantify the safety level of the cell therapy as a function of the number of cells that is needed for the therapy and the type of genome editing that is performed. Even with the highly conservative estimates described here, we anticipate that our solution will rapidly accelerate the entry of cell-based medicine into the clinic.Introduction of a suicide gene together with a linked cell-division gene to generate a safe-cell system enables the selective elimination of proliferating cells after cell transplantation in mouse models of cell therapy.
中文翻译:

连接细胞分裂基因和自杀基因以定义和提高细胞治疗的安全性
人类多能细胞系对开发基于细胞的疗法具有巨大的希望。然而,安全性是临床应用的关键先决条件。许多团体试图通过使用自杀基因来消除潜在的有害细胞,但没有一个团体定量定义移植疗法的安全水平。在这里,我们使用基因组工程策略,证明了自杀系统免受分裂细胞失活的保护。我们在自杀基因单纯疱疹病毒胸苷激酶 (HSV-TK) 和细胞分裂基因 (CDK1) 之间建立了转录联系;这种组合被称为安全单元系统。此外,我们使用数学模型将细胞疗法的安全水平量化为治疗所需的细胞数量和执行的基因组编辑类型的函数。即使采用这里描述的高度保守的估计,我们预计我们的解决方案将迅速加速基于细胞的药物进入临床。将自杀基因与链接的细胞分裂基因一起引入以生成安全细胞系统使在细胞治疗的小鼠模型中细胞移植后选择性消除增殖细胞。
更新日期:2018-11-01
中文翻译:

连接细胞分裂基因和自杀基因以定义和提高细胞治疗的安全性
人类多能细胞系对开发基于细胞的疗法具有巨大的希望。然而,安全性是临床应用的关键先决条件。许多团体试图通过使用自杀基因来消除潜在的有害细胞,但没有一个团体定量定义移植疗法的安全水平。在这里,我们使用基因组工程策略,证明了自杀系统免受分裂细胞失活的保护。我们在自杀基因单纯疱疹病毒胸苷激酶 (HSV-TK) 和细胞分裂基因 (CDK1) 之间建立了转录联系;这种组合被称为安全单元系统。此外,我们使用数学模型将细胞疗法的安全水平量化为治疗所需的细胞数量和执行的基因组编辑类型的函数。即使采用这里描述的高度保守的估计,我们预计我们的解决方案将迅速加速基于细胞的药物进入临床。将自杀基因与链接的细胞分裂基因一起引入以生成安全细胞系统使在细胞治疗的小鼠模型中细胞移植后选择性消除增殖细胞。































 京公网安备 11010802027423号
京公网安备 11010802027423号