Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Aptamer-enabled uptake of small molecule ligands.
Scientific Reports ( IF 3.8 ) Pub Date : 2018-Oct-24 , DOI: 10.1038/s41598-018-33887-w Supipi Liyamali Auwardt , Yeon-Jung Seo , Muslum Ilgu , Judhajeet Ray , Robert R. Feldges , Shambhavi Shubham , Lee Bendickson , Howard A. Levine , Marit Nilsen-Hamilton
Scientific Reports ( IF 3.8 ) Pub Date : 2018-Oct-24 , DOI: 10.1038/s41598-018-33887-w Supipi Liyamali Auwardt , Yeon-Jung Seo , Muslum Ilgu , Judhajeet Ray , Robert R. Feldges , Shambhavi Shubham , Lee Bendickson , Howard A. Levine , Marit Nilsen-Hamilton
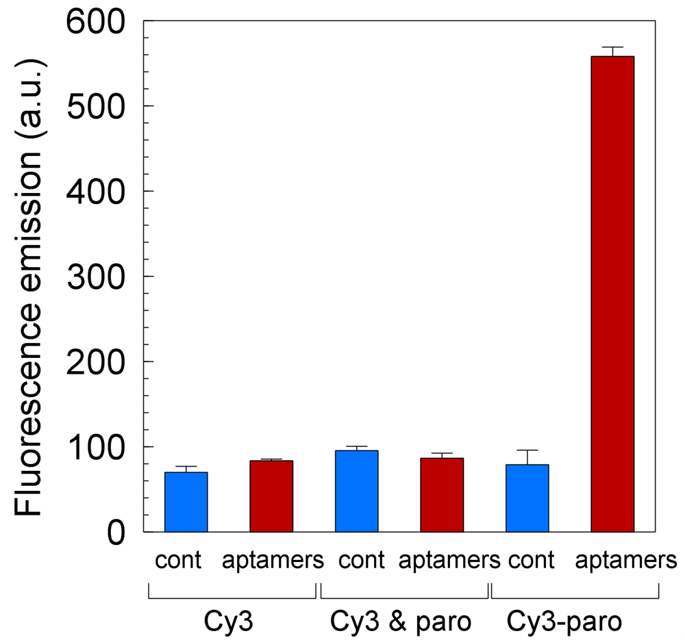
|
The relative ease of isolating aptamers with high specificity for target molecules suggests that molecular recognition may be common in the folds of natural RNAs. We show here that, when expressed in cells, aptamers can increase the intracellular concentrations of their small molecule ligands. We have named these aptamers as DRAGINs (Drug Binding Aptamers for Growing Intracellular Numbers). The DRAGIN property, assessed here by the ability to enhance the toxicity of their ligands, was found for some, but not all, aminoglycoside aptamers. One aptamer protected cells against killing by its ligand. Another aptamer promoted killing as a singlemer and protected against killing as a tandemer. Based on a mathematical model, cell protection vs. killing is proposed as governed by aptamer affinity and access to the inner surface of the cell membrane, with the latter being a critical determinant. With RNA molecules proposed as the earliest functional polymers to drive the evolution of life, we suggest that RNA aptamer-like structures present in primitive cells might have selectively concentrated precursors for polymer synthesis. Riboswitches may be the evolved forms of these ancient aptamer-like "nutrient procurers". Aptamers with DRAGIN capability in the modern world could be applied for imaging cells, in synthetic cell constructs, or to draw drugs into cells to make "undruggable" targets accessible to small molecule inhibitors.
中文翻译:

适体使小分子配体的摄取。
分离对目标分子具有高特异性的适体相对容易,这表明分子识别可能在天然RNA的折叠中很常见。我们在这里表明,当在细胞中表达时,适体可以增加其小分子配体的细胞内浓度。我们将这些适体命名为DRAGIN(用于增加细胞内数目的药物结合适体)。发现了一些但不是全部氨基糖苷适体的DRAGIN性质,其通过增强其配体的毒性的能力来评估。一种适体保护细胞免于被其配体杀死。另一适体促进单分子杀伤并保护其免受单聚体杀伤。根据数学模型,提出了由适体亲和力和进入细胞膜内表面决定细胞保护与杀伤的关系,后者是决定性因素。随着RNA分子被认为是驱动生命进化的最早的功能聚合物,我们建议存在于原始细胞中的RNA适体样结构可能具有选择性浓缩的聚合物合成前体。核糖开关可能是这些古老的适体样“营养素获取者”的进化形式。在现代世界中具有DRAGIN功能的适体可用于细胞成像,合成细胞构建中,或将药物吸入细胞以使小分子抑制剂可接近“不可药物”靶标。我们建议存在于原始细胞中的RNA适体样结构可能具有用于聚合物合成的选择性浓缩前体。核糖开关可能是这些古老的适体样“营养素获取者”的进化形式。在现代世界中具有DRAGIN功能的适体可用于细胞成像,合成细胞构建中,或将药物吸入细胞以使小分子抑制剂可接近“不可药物”靶标。我们建议存在于原始细胞中的RNA适体样结构可能具有用于聚合物合成的选择性浓缩前体。核糖开关可能是这些古老的适体样“营养素获取者”的进化形式。在现代世界中具有DRAGIN功能的适体可用于细胞成像,合成细胞构建中,或将药物吸入细胞以使小分子抑制剂可接近“不可药物”靶标。
更新日期:2018-10-24
中文翻译:

适体使小分子配体的摄取。
分离对目标分子具有高特异性的适体相对容易,这表明分子识别可能在天然RNA的折叠中很常见。我们在这里表明,当在细胞中表达时,适体可以增加其小分子配体的细胞内浓度。我们将这些适体命名为DRAGIN(用于增加细胞内数目的药物结合适体)。发现了一些但不是全部氨基糖苷适体的DRAGIN性质,其通过增强其配体的毒性的能力来评估。一种适体保护细胞免于被其配体杀死。另一适体促进单分子杀伤并保护其免受单聚体杀伤。根据数学模型,提出了由适体亲和力和进入细胞膜内表面决定细胞保护与杀伤的关系,后者是决定性因素。随着RNA分子被认为是驱动生命进化的最早的功能聚合物,我们建议存在于原始细胞中的RNA适体样结构可能具有选择性浓缩的聚合物合成前体。核糖开关可能是这些古老的适体样“营养素获取者”的进化形式。在现代世界中具有DRAGIN功能的适体可用于细胞成像,合成细胞构建中,或将药物吸入细胞以使小分子抑制剂可接近“不可药物”靶标。我们建议存在于原始细胞中的RNA适体样结构可能具有用于聚合物合成的选择性浓缩前体。核糖开关可能是这些古老的适体样“营养素获取者”的进化形式。在现代世界中具有DRAGIN功能的适体可用于细胞成像,合成细胞构建中,或将药物吸入细胞以使小分子抑制剂可接近“不可药物”靶标。我们建议存在于原始细胞中的RNA适体样结构可能具有用于聚合物合成的选择性浓缩前体。核糖开关可能是这些古老的适体样“营养素获取者”的进化形式。在现代世界中具有DRAGIN功能的适体可用于细胞成像,合成细胞构建中,或将药物吸入细胞以使小分子抑制剂可接近“不可药物”靶标。















































 京公网安备 11010802027423号
京公网安备 11010802027423号