当前位置:
X-MOL 学术
›
Mol. Pharmaceutics
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
抗体CDR残基对化学修饰的敏感性可以在潜在的抗体人源化和辅助选择过程中揭示出来
Molecular Pharmaceutics ( IF 4.5 ) Pub Date : 2018-08-17 00:00:00 , DOI: 10.1021/acs.molpharmaceut.8b00536 Ankai Xu , Hok Seon Kim , Samarkand Estee , Sharon ViaJar , William J. Galush , Avinash Gill , Isidro Hötzel , Greg A. Lazar , Paul McDonald , Nisana Andersen , Christoph Spiess
Molecular Pharmaceutics ( IF 4.5 ) Pub Date : 2018-08-17 00:00:00 , DOI: 10.1021/acs.molpharmaceut.8b00536 Ankai Xu , Hok Seon Kim , Samarkand Estee , Sharon ViaJar , William J. Galush , Avinash Gill , Isidro Hötzel , Greg A. Lazar , Paul McDonald , Nisana Andersen , Christoph Spiess
|
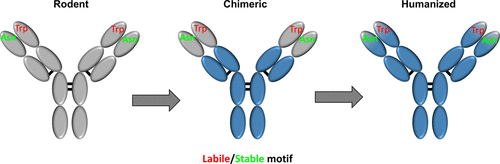
治疗性抗体的临床开发路径的关键部分涉及评估整个制造过程中候选分子的物理和化学稳定性。特别地,需要通过制剂开发来控制可能影响抗原结合的化学负债的风险,例如脱酰胺,氧化和异构化,以消除抗体CDR序列中的风险,或者通过替换显示化学不稳定性的氨基酸基序来消除这种风险。通常,抗体CDR序列包含多个用于化学不稳定的序列基序(潜在热点)。但是,这些基序中只有一个子集会导致实际的化学修饰,因此,需要进行不稳定性程度的实验评估才能确定潜在序列工程的位置。理想情况下,在亲本啮齿动物抗体鉴定阶段,在抗体人源化之前,应该可以使用此信息。对责任的早期了解允许通过与抗体人源化过程的并发工程而不是耗时的顺序活动来对克隆进行排名或减轻责任。然而,化学责任和人源化的同时工程要求从啮齿动物亲本抗体到人源化的化学修饰的可翻译性。我们通过在啮齿动物亲本抗体和最终人源化抗体之间进行质谱肽图分析,比较了所有序列基序的稳定性,并观察到线性相关性。

"点击查看英文标题和摘要"
更新日期:2018-08-17

"点击查看英文标题和摘要"





















































 京公网安备 11010802027423号
京公网安备 11010802027423号