当前位置:
X-MOL 学术
›
EMBO Mol. Med.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
HIF-LIMD1负反馈机制减轻缺氧的促肿瘤作用
EMBO Molecular Medicine ( IF 9.0 ) Pub Date : 2018-08-01 , DOI: 10.15252/emmm.201708304 Daniel E Foxler, Katherine S Bridge, John G Foster, Paul Grevitt, Sean Curry, Kunal M Shah, Kathryn M Davidson, Ai Nagano, Emanuela Gadaleta, Hefin I Rhys, Paul T Kennedy, Miguel A Hermida, Ting‐Yu Chang, Peter E Shaw, Louise E Reynolds, Tristan R McKay, Hsei‐Wei Wang, Paulo S Ribeiro, Michael J Plevin, Dimitris Lagos, Nicholas R Lemoine, Prabhakar Rajan, Trevor A Graham, Claude Chelala, Kairbaan M Hodivala‐Dilke, Ian Spendlove, Tyson V Sharp
|
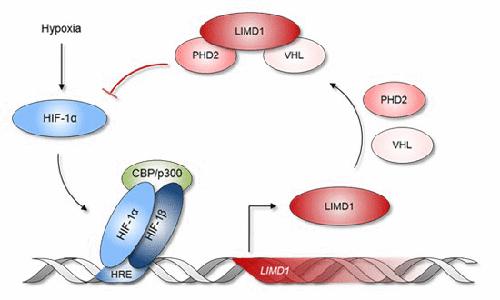
细胞对低氧张力的适应性反应是由缺氧诱导因子 ( HIF ) 介导的,HIF 是由HIF -α 和HIF -β 亚基组成的异二聚体转录因子家族。 HIF长时间表达是细胞转化、肿瘤发生和转移的关键因素。因此,缺氧条件下HIF 的降解是一种重要的稳态和肿瘤抑制机制。 LIMD 1 在生理氧水平(含氧量正常)下与PHD 2 和VHL形成复合物,以促进HIF ‐α 亚基的蛋白酶体降解。在这里,我们将LIMD 1确定为HIF ‐1 靶基因,它通过调节PHD 2- LIMD 1- VHL复合物的形成来介导以前未表征的负调节反馈机制,以促进缺氧HIF ‐α 降解。低氧诱导LIMD 1表达导致HIF ‐α 蛋白降解增加,抑制HIF ‐1 靶基因表达、肿瘤生长和血管形成。此外,我们报告LIMD 1位点的拷贝数变异发生在 47.1% 的肺腺癌患者中,与HIF靶基因特征的表达增强相关,并且是一个负面预后指标。总而言之,我们的数据开辟了LIMD 1阴性肺癌的病因学、诊断和预后的新研究领域。

"点击查看英文标题和摘要"





























 京公网安备 11010802027423号
京公网安备 11010802027423号