当前位置:
X-MOL 学术
›
J. Phys. Chem. B
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Mechanism for Fluorescence Quenching of Tryptophan by Oxamate and Pyruvate: Conjugation and Solvation-Induced Photoinduced Electron Transfer
The Journal of Physical Chemistry B ( IF 2.8 ) Pub Date : 2018-06-15 , DOI: 10.1021/acs.jpcb.8b02433 Huo-Lei Peng 1 , Robert Callender 1
The Journal of Physical Chemistry B ( IF 2.8 ) Pub Date : 2018-06-15 , DOI: 10.1021/acs.jpcb.8b02433 Huo-Lei Peng 1 , Robert Callender 1
Affiliation
|
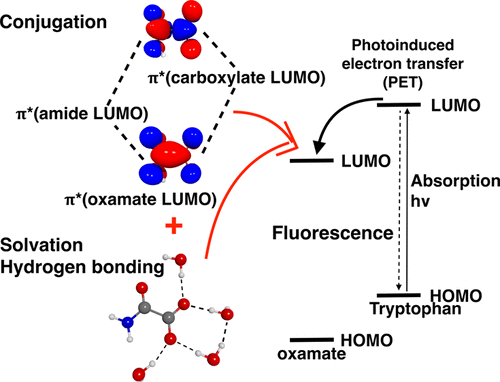
Oxamate and pyruvate are isoelectronic molecules. They both quench tryptophan fluorescence with Stern–Volmer constants of 16 and 20 M–1, respectively, which are comparable to that of arcrylamide, a commonly used probe for protein structure. On the other hand, it is well known that neither the carboxylate group of these molecules nor the amide group is a good quencher. To find the mechanism of the quenching by oxamate and pyruvate, density functional theory computations with a polarizable continuum model, solvation based on density, and explicit waters, were performed. Results indicate that both molecules can be an electron acceptor via photoinduced electron transfer. There are two requirements. First, the carboxylate and amide moieties must be in direct contact to bring about noticeable quenching. The conjugation between the amide (or the keto) group and the carboxylate group leads to a lower π* orbital, which is the lowest unoccupied molecular orbital (LUMO), and can then accept an electron from the excited tryptophan. Second, since oxamate and pyruvate ions have high electron density, hydrogen bonds with waters, which can be simulated by an explicit water model, are essential. Their LUMO energies are strongly influenced by water in aqueous solution. The above findings demonstrate how tryptophan fluorescence gets quenched in aqueous solution. The findings may be important in dealing with those problems where frontier orbitals are considered, especially with molecules having high electron density.
中文翻译:

草酸盐和丙酮酸对色氨酸的荧光猝灭机理:共轭和溶剂化诱导的光诱导电子转移
草酸盐和丙酮酸盐是等电子分子。他们都用16和20 M –1的Stern–Volmer常数猝灭色氨酸荧光。分别与蛋白质结构的常用探针Arcrylamide相当。另一方面,众所周知,这些分子的羧酸酯基团和酰胺基团都不是良好的淬灭剂。为了找到草酸盐和丙酮酸猝灭的机理,进行了可极化连续体模型的密度泛函理论计算,基于密度的溶剂化和显性水。结果表明,两个分子都可以通过光诱导的电子转移成为电子受体。有两个要求。首先,羧酸酯和酰胺部分必须直接接触以引起明显的猝灭。酰胺基(或酮基)和羧酸酯基之间的共轭导致较低的π*轨道,这是最低的未占据分子轨道(LUMO),然后可以从激发的色氨酸接收电子。其次,由于草酸盐和丙酮酸离子具有高电子密度,因此与水的氢键(可以通过显式水模型进行模拟)是必不可少的。它们的LUMO能量受水溶液中水的强烈影响。以上发现证明了色氨酸荧光如何在水溶液中猝灭。该发现对于解决那些考虑前沿轨道的问题可能是重要的,尤其是对于具有高电子密度的分子而言。以上发现证明了色氨酸荧光如何在水溶液中猝灭。该发现对于解决那些考虑前沿轨道的问题可能是重要的,尤其是对于具有高电子密度的分子而言。以上发现证明了色氨酸荧光如何在水溶液中猝灭。该发现对于解决那些考虑前沿轨道的问题可能是重要的,尤其是对于具有高电子密度的分子而言。
更新日期:2018-06-15
中文翻译:

草酸盐和丙酮酸对色氨酸的荧光猝灭机理:共轭和溶剂化诱导的光诱导电子转移
草酸盐和丙酮酸盐是等电子分子。他们都用16和20 M –1的Stern–Volmer常数猝灭色氨酸荧光。分别与蛋白质结构的常用探针Arcrylamide相当。另一方面,众所周知,这些分子的羧酸酯基团和酰胺基团都不是良好的淬灭剂。为了找到草酸盐和丙酮酸猝灭的机理,进行了可极化连续体模型的密度泛函理论计算,基于密度的溶剂化和显性水。结果表明,两个分子都可以通过光诱导的电子转移成为电子受体。有两个要求。首先,羧酸酯和酰胺部分必须直接接触以引起明显的猝灭。酰胺基(或酮基)和羧酸酯基之间的共轭导致较低的π*轨道,这是最低的未占据分子轨道(LUMO),然后可以从激发的色氨酸接收电子。其次,由于草酸盐和丙酮酸离子具有高电子密度,因此与水的氢键(可以通过显式水模型进行模拟)是必不可少的。它们的LUMO能量受水溶液中水的强烈影响。以上发现证明了色氨酸荧光如何在水溶液中猝灭。该发现对于解决那些考虑前沿轨道的问题可能是重要的,尤其是对于具有高电子密度的分子而言。以上发现证明了色氨酸荧光如何在水溶液中猝灭。该发现对于解决那些考虑前沿轨道的问题可能是重要的,尤其是对于具有高电子密度的分子而言。以上发现证明了色氨酸荧光如何在水溶液中猝灭。该发现对于解决那些考虑前沿轨道的问题可能是重要的,尤其是对于具有高电子密度的分子而言。































 京公网安备 11010802027423号
京公网安备 11010802027423号