当前位置:
X-MOL 学术
›
Cell Death Dis.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
ADAR1介导的A-to-I RNA编辑丢失后的细胞死亡不受内在凋亡途径的影响。
Cell Death & Disease ( IF 8.1 ) Pub Date : 2019-12-04 , DOI: 10.1038/s41419-019-2160-6
Carl R Walkley 1, 2, 3 , Benjamin T Kile 4, 5
Cell Death & Disease ( IF 8.1 ) Pub Date : 2019-12-04 , DOI: 10.1038/s41419-019-2160-6
Carl R Walkley 1, 2, 3 , Benjamin T Kile 4, 5
Affiliation
|
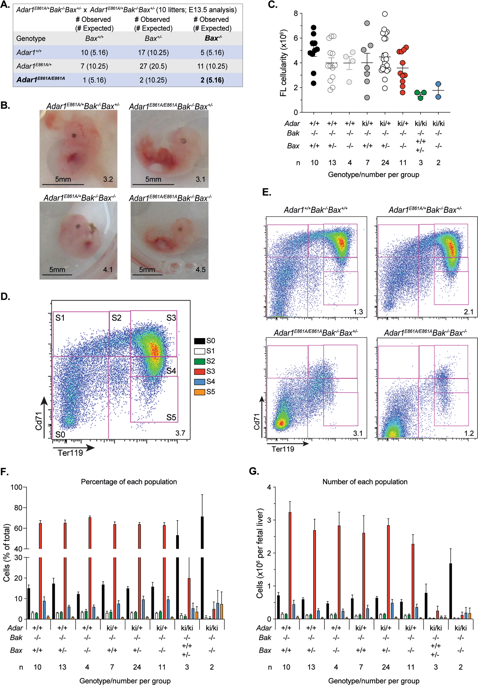
RNA的修饰(统称为表观转录组)广泛存在,在进化上是保守的,并且有助于健康和疾病状态下的基因调节和蛋白质多样性。描述了超过160种RNA修饰,大大超过了DNA修饰的数量。其中,腺苷到肌苷(A到I)的RNA编辑是最常见的一种。鼠标中有成千上万个A-to-I编辑站点,而人类中则有数百万个。翻译或测序后,肌苷碱基被解码为鸟苷,导致RNA和DNA之间的A到G错配。肌苷与腺苷具有不同的碱基配对特性,因此编辑不仅会改变RNA编码,而且还会改变RNA结构。在哺乳动物中,ADAR1和ADAR2进行A对I编辑。小鼠功能ADAR1等位基因丧失的特征是细胞死亡和无法存活的胚胎发生。Adar1-/-和编辑缺陷型(Adar1E861A / E861A)小鼠在造血功能衰竭的E11.75-13.5之间死亡。令人惊讶的是,该表型通过胞质dsRNA传感器MDA5或其下游衔接子MAVS的缺失而得以挽救,这种机制在人和小鼠中都得到了保留。当前文献表明,ADAR1的丢失通过细胞凋亡导致细胞死亡,但是这尚未在遗传学上得到证实。我们报告说,内在的(线粒体)凋亡途径的阻断通过BAK和BAX的丢失,不会挽救或改变胎儿肝脏的细胞表型,也不会延长ADAR1编辑缺陷胚胎的寿命。我们曾预计,BAK和BAX的损失将挽救或至少大大延长 Adar1E861A / E861A胚胎的孕育能力。但是,在E13.5恢复的三重突变型Adar1E861A / E861A Bak-/-Bax-/-胚胎与带有BAK和BAX的Adar1E861A / E861A胚胎没有区别。结果表明,不需要内在凋亡途径的细胞死亡过程是由ADAR1丢失后的MDA5触发的。

"点击查看英文标题和摘要"
更新日期:2019-12-04

"点击查看英文标题和摘要"

































 京公网安备 11010802027423号
京公网安备 11010802027423号