当前位置:
X-MOL 学术
›
Microchim. Acta
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Electrochemiluminescence immunoassay for the N-terminal pro-B-type natriuretic peptide based on resonance energy transfer between a self-enhanced luminophore composed of silver nanocubes on gold nanoparticles and a metal-organic framework of type MIL-125
Microchimica Acta ( IF 5.3 ) Pub Date : 2019-11-19 , DOI: 10.1007/s00604-019-3969-5 Xue Dong 1 , Guanhui Zhao 1 , Xuan Li 1 , JunCong Miao 1 , Jinglong Fang 1 , Qin Wei 1 , Wei Cao 1
Microchimica Acta ( IF 5.3 ) Pub Date : 2019-11-19 , DOI: 10.1007/s00604-019-3969-5 Xue Dong 1 , Guanhui Zhao 1 , Xuan Li 1 , JunCong Miao 1 , Jinglong Fang 1 , Qin Wei 1 , Wei Cao 1
Affiliation
|
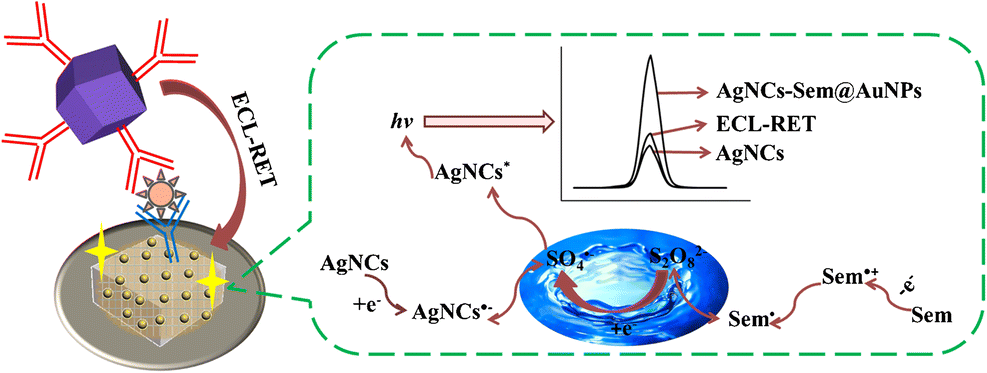
The N-terminal pro-B-type natriuretic peptide (NT-proBNP) is a marker of heart failure. A novel sandwich type electrochemiluminescence (ECL) immunoassay is described for the NT-proBNP. The method is based on ECL resonance energy transfer (RET) between silver nanocubes that were covered with semicarbazide-modified gold nanoparticles (AgNC-sem@AuNPs) as the donor, and a Ti(IV)-based metal-organic framework of type MIL-125 as the acceptor. The ECL signal was strongly amplified by increasing the luminous efficiency. ECL-RET occurs due to the partial overlap between the ECL emission of the AgNC-sem@AuNPs (emission wavelength at 470 nm to 900 nm) and the visible absorption spectrum of MIL-125 (absorption wavelength at 406 nm to 900 nm). This results in the quenching of ECL. The AgNC-sem@AuNPs were placed on the electrode. The antibody was immobilized on AgNC-sem@AuNPs via Au-NH2 bond, and MIL-125 was utilized as a label for the secondary antibody. The assay works in the 0.25 pg mL−1 to 100 ng mL−1 concentration range and has a 0.11 pg mL−1 lower detection limit (at S/N = 3). Graphical abstract Schematic representation of self-enhanced luminescence mechanism (semicarbazide (Sem) as co-reaction accelerator) and Electrochemiluminescence resonance energy transfer (ECL-RET): silver nanocubes (AgNCs) as the energy donor and MIL-125 as the energy acceptor. Schematic representation of self-enhanced luminescence mechanism (semicarbazide (Sem) as co-reaction accelerator) and Electrochemiluminescence resonance energy transfer (ECL-RET): silver nanocubes (AgNCs) as the energy donor and MIL-125 as the energy acceptor.
中文翻译:

基于由金纳米颗粒上的银纳米立方体组成的自增强发光团与 MIL-125 型金属有机框架之间共振能量转移的 N 端前 B 型利钠肽的电化学发光免疫测定
N 端 B 型利钠肽原 (NT-proBNP) 是心力衰竭的标志物。一种新型夹心型电化学发光 (ECL) 免疫测定被描述为 NT-proBNP。该方法基于覆盖有氨基脲修饰的金纳米粒子(AgNC-sem@AuNPs)作为供体的银纳米立方体与基于Ti(IV)的MIL型金属有机框架之间的ECL共振能量转移(RET) -125 作为接受者。通过提高发光效率,ECL 信号被强烈放大。ECL-RET 的发生是由于 AgNC-sem@AuNPs 的 ECL 发射(发射波长为 470 nm 至 900 nm)与 MIL-125 的可见吸收光谱(吸收波长为 406 nm 至 900 nm)之间的部分重叠。这导致 ECL 的淬灭。AgNC-sem@AuNPs 被放置在电极上。抗体通过 Au-NH2 键固定在 AgNC-sem@AuNPs 上,MIL-125 用作二抗的标记。该测定在 0.25 pg mL-1 至 100 ng mL-1 浓度范围内工作,检测下限为 0.11 pg mL-1(S/N = 3)。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。并且 MIL-125 被用作二抗的标记。该测定在 0.25 pg mL-1 至 100 ng mL-1 浓度范围内工作,检测下限为 0.11 pg mL-1(S/N = 3)。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。并且 MIL-125 被用作二抗的标记。该测定在 0.25 pg mL-1 至 100 ng mL-1 浓度范围内工作,检测下限为 0.11 pg mL-1(S/N = 3)。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。11 pg mL-1 检测下限(S/N = 3)。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。11 pg mL-1 检测下限(S/N = 3)。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。
更新日期:2019-11-19
中文翻译:

基于由金纳米颗粒上的银纳米立方体组成的自增强发光团与 MIL-125 型金属有机框架之间共振能量转移的 N 端前 B 型利钠肽的电化学发光免疫测定
N 端 B 型利钠肽原 (NT-proBNP) 是心力衰竭的标志物。一种新型夹心型电化学发光 (ECL) 免疫测定被描述为 NT-proBNP。该方法基于覆盖有氨基脲修饰的金纳米粒子(AgNC-sem@AuNPs)作为供体的银纳米立方体与基于Ti(IV)的MIL型金属有机框架之间的ECL共振能量转移(RET) -125 作为接受者。通过提高发光效率,ECL 信号被强烈放大。ECL-RET 的发生是由于 AgNC-sem@AuNPs 的 ECL 发射(发射波长为 470 nm 至 900 nm)与 MIL-125 的可见吸收光谱(吸收波长为 406 nm 至 900 nm)之间的部分重叠。这导致 ECL 的淬灭。AgNC-sem@AuNPs 被放置在电极上。抗体通过 Au-NH2 键固定在 AgNC-sem@AuNPs 上,MIL-125 用作二抗的标记。该测定在 0.25 pg mL-1 至 100 ng mL-1 浓度范围内工作,检测下限为 0.11 pg mL-1(S/N = 3)。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。并且 MIL-125 被用作二抗的标记。该测定在 0.25 pg mL-1 至 100 ng mL-1 浓度范围内工作,检测下限为 0.11 pg mL-1(S/N = 3)。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。并且 MIL-125 被用作二抗的标记。该测定在 0.25 pg mL-1 至 100 ng mL-1 浓度范围内工作,检测下限为 0.11 pg mL-1(S/N = 3)。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。11 pg mL-1 检测下限(S/N = 3)。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。11 pg mL-1 检测下限(S/N = 3)。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。自增强发光机制(氨基脲(Sem)作为共反应加速器)和电化学发光共振能量转移(ECL-RET)的示意图:银纳米立方体(AgNCs)作为能量供体,MIL-125作为能量受体。





















































 京公网安备 11010802027423号
京公网安备 11010802027423号