当前位置:
X-MOL 学术
›
Nat. Rev. Immunol.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Tumour-intrinsic resistance to immune checkpoint blockade.
Nature Reviews Immunology ( IF 67.7 ) Pub Date : 2019-09-30 , DOI: 10.1038/s41577-019-0218-4 Anusha Kalbasi 1, 2, 3, 4 , Antoni Ribas 2, 3, 4, 5, 6
Nature Reviews Immunology ( IF 67.7 ) Pub Date : 2019-09-30 , DOI: 10.1038/s41577-019-0218-4 Anusha Kalbasi 1, 2, 3, 4 , Antoni Ribas 2, 3, 4, 5, 6
Affiliation
|
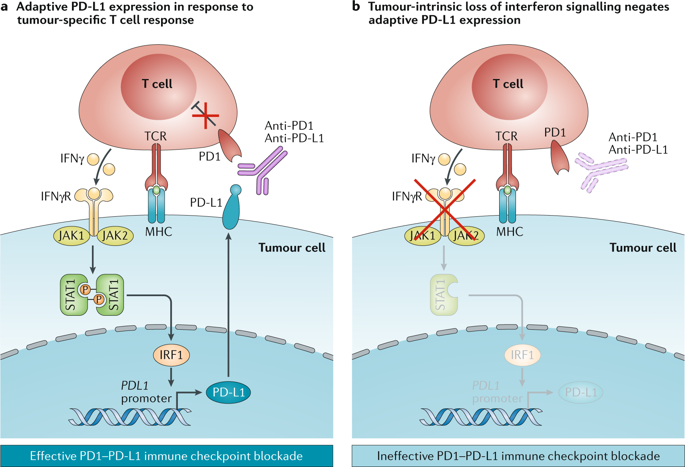
'Immune checkpoint blockade' for cancer describes the use of therapeutic antibodies that disrupt negative immune regulatory checkpoints and unleash pre-existing antitumour immune responses. Antibodies targeting the checkpoint molecules cytotoxic T lymphocyte antigen 4 (CTLA4), programmed cell death 1 (PD1) and PD1 ligand 1 (PD-L1) have had early success in the clinic, which has led to approval by the US Food and Drug Administration of multiple agents in several cancer types. Yet, clinicians still have very limited tools to discriminate a priori patients who will and will not respond to treatment. This has fuelled a wave of research into the molecular mechanisms of tumour-intrinsic resistance to immune checkpoint blockade, leading to the rediscovery of biological processes critical to antitumour immunity, namely interferon signalling and antigen presentation. Other efforts have shed light on the immunological implications of canonical cancer signalling pathways, such as WNT-β-catenin signalling, cell cycle regulatory signalling, mitogen-activated protein kinase signalling and pathways activated by loss of the tumour suppressor phosphoinositide phosphatase PTEN. Here we review each of these molecular mechanisms of resistance and explore ongoing approaches to overcome resistance to immune checkpoint blockade and expand the spectrum of patients who can benefit from immune checkpoint blockade.
中文翻译:

对免疫检查点阻断的肿瘤内在抗性。
癌症的“免疫检查点封锁”描述了使用治疗性抗体破坏负免疫调节检查点并释放预先存在的抗肿瘤免疫反应。针对检查点分子细胞毒性 T 淋巴细胞抗原 4 (CTLA4)、程序性细胞死亡 1 (PD1) 和 PD1 配体 1 (PD-L1) 的抗体在临床上取得了早期成功,并获得了美国食品和药物管理局的批准在几种癌症类型中使用多种药物。然而,临床医生仍然拥有非常有限的工具来区分对治疗有反应和不会有反应的先验患者。这推动了对免疫检查点阻断的肿瘤内在抗性分子机制的研究浪潮,导致重新发现对抗肿瘤免疫至关重要的生物过程,即干扰素信号传导和抗原呈递。其他努力阐明了典型癌症信号通路的免疫学意义,例如 WNT-β-连环蛋白信号通路、细胞周期调节信号通路、丝裂原活化蛋白激酶信号通路和肿瘤抑制因子磷酸肌醇磷酸酶 PTEN 缺失激活的通路。在这里,我们回顾了这些耐药性分子机制中的每一个,并探索了克服免疫检查点封锁耐药性的持续方法,并扩大了可以从免疫检查点封锁中受益的患者范围。丝裂原活化蛋白激酶信号传导和由肿瘤抑制因子磷酸肌醇磷酸酶 PTEN 缺失激活的通路。在这里,我们回顾了这些耐药性分子机制中的每一个,并探索了克服免疫检查点封锁耐药性的持续方法,并扩大了可以从免疫检查点封锁中受益的患者范围。丝裂原活化蛋白激酶信号传导和由肿瘤抑制因子磷酸肌醇磷酸酶 PTEN 缺失激活的通路。在这里,我们回顾了这些耐药性分子机制中的每一个,并探索了克服免疫检查点封锁耐药性的持续方法,并扩大了可以从免疫检查点封锁中受益的患者范围。
更新日期:2019-09-30
中文翻译:

对免疫检查点阻断的肿瘤内在抗性。
癌症的“免疫检查点封锁”描述了使用治疗性抗体破坏负免疫调节检查点并释放预先存在的抗肿瘤免疫反应。针对检查点分子细胞毒性 T 淋巴细胞抗原 4 (CTLA4)、程序性细胞死亡 1 (PD1) 和 PD1 配体 1 (PD-L1) 的抗体在临床上取得了早期成功,并获得了美国食品和药物管理局的批准在几种癌症类型中使用多种药物。然而,临床医生仍然拥有非常有限的工具来区分对治疗有反应和不会有反应的先验患者。这推动了对免疫检查点阻断的肿瘤内在抗性分子机制的研究浪潮,导致重新发现对抗肿瘤免疫至关重要的生物过程,即干扰素信号传导和抗原呈递。其他努力阐明了典型癌症信号通路的免疫学意义,例如 WNT-β-连环蛋白信号通路、细胞周期调节信号通路、丝裂原活化蛋白激酶信号通路和肿瘤抑制因子磷酸肌醇磷酸酶 PTEN 缺失激活的通路。在这里,我们回顾了这些耐药性分子机制中的每一个,并探索了克服免疫检查点封锁耐药性的持续方法,并扩大了可以从免疫检查点封锁中受益的患者范围。丝裂原活化蛋白激酶信号传导和由肿瘤抑制因子磷酸肌醇磷酸酶 PTEN 缺失激活的通路。在这里,我们回顾了这些耐药性分子机制中的每一个,并探索了克服免疫检查点封锁耐药性的持续方法,并扩大了可以从免疫检查点封锁中受益的患者范围。丝裂原活化蛋白激酶信号传导和由肿瘤抑制因子磷酸肌醇磷酸酶 PTEN 缺失激活的通路。在这里,我们回顾了这些耐药性分子机制中的每一个,并探索了克服免疫检查点封锁耐药性的持续方法,并扩大了可以从免疫检查点封锁中受益的患者范围。































 京公网安备 11010802027423号
京公网安备 11010802027423号