当前位置:
X-MOL 学术
›
Cell Death Dis.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
DPP8 / 9抑制剂是功能性NLRP1等位基因的通用激活剂。
Cell Death & Disease ( IF 8.1 ) Pub Date : 2019-08-05 , DOI: 10.1038/s41419-019-1817-5 Kuo Gai 1 , Marian C Okondo 1 , Sahana D Rao 2 , Ashley J Chui 2 , Daniel P Ball 1 , Darren C Johnson 2 , Daniel A Bachovchin 1, 2, 3
Cell Death & Disease ( IF 8.1 ) Pub Date : 2019-08-05 , DOI: 10.1038/s41419-019-1817-5 Kuo Gai 1 , Marian C Okondo 1 , Sahana D Rao 2 , Ashley J Chui 2 , Daniel P Ball 1 , Darren C Johnson 2 , Daniel A Bachovchin 1, 2, 3
Affiliation
|
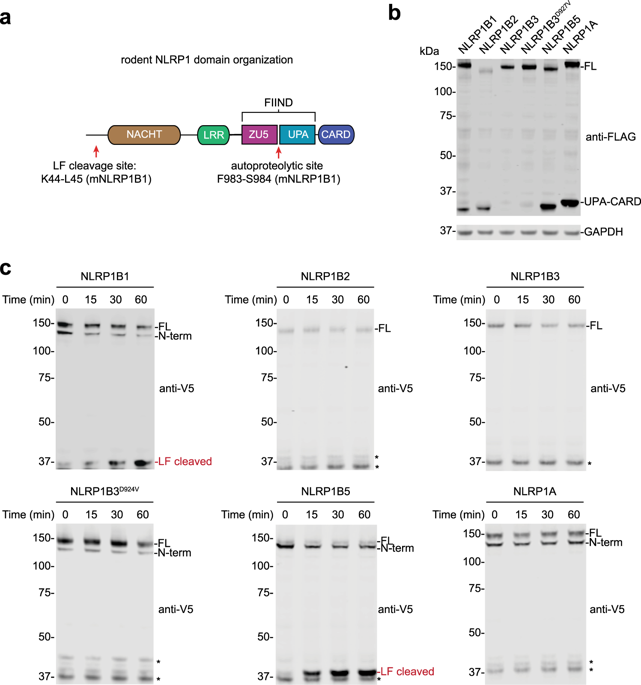
细胞内的致病结构或活性刺激炎症小体的形成,这些炎症小体募集并激活caspase-1,并触发炎性形式的细胞死亡,称为焦磷酸化。众所周知,哺乳动物的炎症小体传感器蛋白都可以检测一种特定类型的信号,例如双链DNA或细菌鞭毛蛋白。值得注意的是,NLRP1是第一个被发现形成炎症小体的蛋白质,但尚未确定NLRP1检测到的致病信号。NLRP1是高度多态的,即使在近交啮齿动物品系中也是如此,并且已经表明这些多样化的NLRP1等位基因可能已经进化为检测完全不同的刺激。有趣的是,最近显示丝氨酸蛋白酶DPP8和DPP9(DPP8 / 9)的抑制剂可激活人NLRP1,其同系物CARD8和几个小鼠NLRP1等位基因。这里,我们现在显示DPP8 / 9抑制剂激活了所有功能性啮齿动物NLRP1等位基因,表明DPP8 / 9抑制作用诱导了所有NLRP1蛋白检测到的信号。此外,我们发现NLRP1等位基因对DPP8 / 9抑制剂诱导的弓形虫和弓形虫诱导的凋亡的敏感性非常相似,这表明DPP8 / 9抑制表型是弓形虫的关键活性。总的来说,这项工作表明,高度多态的NLRP1炎性小体确实像其他哺乳动物的炎性小体一样感觉到特定的信号。提示DPP8 / 9抑制表型是弓形虫的关键活性。总体而言,这项工作表明,高度多态的NLRP1炎性小体确实像其他哺乳动物的炎性小体一样能感知特定的信号。提示DPP8 / 9抑制表型是弓形虫的关键活性。总体而言,这项工作表明,高度多态的NLRP1炎性小体确实像其他哺乳动物的炎性小体一样能感知特定的信号。

"点击查看英文标题和摘要"
更新日期:2019-08-05

"点击查看英文标题和摘要"































 京公网安备 11010802027423号
京公网安备 11010802027423号