Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
破骨细胞的发育起源、功能维持和基因拯救
Nature ( IF 50.5 ) Pub Date : 2019-04-01 , DOI: 10.1038/s41586-019-1105-7
Christian E Jacome-Galarza 1 , Gulce I Percin 2, 3 , James T Muller 1 , Elvira Mass 1, 4 , Tomi Lazarov 1 , Jiri Eitler 2 , Martina Rauner 5 , Vijay K Yadav 6 , Lucile Crozet 1 , Mathieu Bohm 1 , Pierre-Louis Loyher 1 , Gerard Karsenty 6 , Claudia Waskow 2, 3, 5 , Frederic Geissmann 1
Nature ( IF 50.5 ) Pub Date : 2019-04-01 , DOI: 10.1038/s41586-019-1105-7
Christian E Jacome-Galarza 1 , Gulce I Percin 2, 3 , James T Muller 1 , Elvira Mass 1, 4 , Tomi Lazarov 1 , Jiri Eitler 2 , Martina Rauner 5 , Vijay K Yadav 6 , Lucile Crozet 1 , Mathieu Bohm 1 , Pierre-Louis Loyher 1 , Gerard Karsenty 6 , Claudia Waskow 2, 3, 5 , Frederic Geissmann 1
Affiliation
|
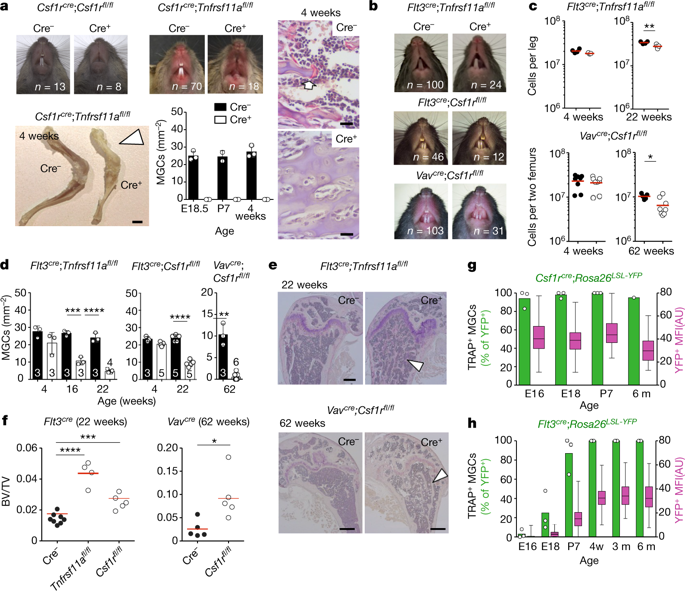
破骨细胞是多核巨细胞,可吸收骨骼,确保骨骼和骨髓造血生态位的发育和持续重塑。破骨细胞活性缺陷会导致骨硬化症和骨髓衰竭 1-9,而过度活性会导致骨质流失和骨质疏松症 10。骨硬化症可以通过人类和小鼠的骨髓移植部分治疗 11-18,这与破骨细胞的造血起源一致 13,16,19 和研究表明,它们是通过在 CSF1 和RANK 配体 1,20。然而,破骨细胞的发育起源和寿命,以及在体内确保破骨细胞功能维持的机制在很大程度上仍未被探索。在这里,我们报告定殖胎儿骨化中心的破骨细胞起源于胚胎红细胞 - 骨髓祖细胞21, 22。这些红细胞-骨髓祖细胞衍生的破骨细胞是正常骨骼发育和牙齿萌出所必需的。然而,在新生小鼠中及时输注造血干细胞衍生的单核细胞足以挽救早发性常染色体隐性骨硬化症的骨骼发育。我们还发现,破骨细胞、骨量和骨髓腔的产后维持涉及循环血单核细胞与长寿命破骨细胞合胞体的迭代融合。因此,在没有造血干细胞嵌合的情况下,单核细胞的联体共生或输血导致破骨细胞中的长期基因转移,并且可以挽救由组织蛋白酶 K 缺乏引起的成人发病的骨硬化表型23, 24。总之,我们的研究结果确定了破骨细胞的发育起源以及控制它们在出生后在骨骼中维持的机制。这些数据提出了在骨硬化症中挽救破骨细胞缺乏和调节体内破骨细胞活性的策略。小鼠正常骨骼发育和牙齿萌出所需的多核破骨细胞来源于胚胎红髓细胞祖细胞,并在出生后通过与循环单核细胞融合而维持。

"点击查看英文标题和摘要"
更新日期:2019-04-01

"点击查看英文标题和摘要"

































 京公网安备 11010802027423号
京公网安备 11010802027423号