当前位置:
X-MOL 学术
›
Neuropharmacology
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
KCC2 membrane diffusion tunes neuronal chloride homeostasis.
Neuropharmacology ( IF 4.6 ) Pub Date : 2019-03-11 , DOI: 10.1016/j.neuropharm.2019.03.014 Etienne Côme 1 , Xavier Marques 1 , Jean Christophe Poncer 1 , Sabine Lévi 1
Neuropharmacology ( IF 4.6 ) Pub Date : 2019-03-11 , DOI: 10.1016/j.neuropharm.2019.03.014 Etienne Côme 1 , Xavier Marques 1 , Jean Christophe Poncer 1 , Sabine Lévi 1
Affiliation
|
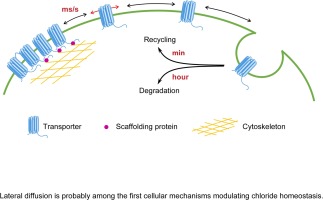
Neuronal Cl- homeostasis is regulated by the activity of two cation chloride co-transporters (CCCs), the K+-Cl- cotransporter KCC2 and the Na+-K+-Cl- cotransporter NKCC1, which are primarily extruding and importing chloride in neurons, respectively. Several neurological and psychiatric disorders including epilepsy, neuropathic pain, schizophrenia and autism are associated with altered neuronal chloride (Cl-) homeostasis. A current view is that the accumulation of intracellular Cl- in neurons as a result of KCC2 down-regulation and/or NKCC1 up-regulation may weaken inhibitory GABA signaling and thereby promote the development of pathological activities. CCC activity is determined mainly by their level of expression in the plasma membrane. Furthermore, CCCs undergo "diffusion-trapping" in the membrane, a mechanism that is rapidly adjusted by activity-dependent post-translational modifications i.e. phosphorylation/dephosphorylation of key serine and threonine residues. This represents probably the most rapid cellular mechanism for adapting CCC function to changes in neuronal activity. Therefore, interfering with these mechanisms may help restoring Cl- homeostasis and inhibition under pathological conditions. This article is part of the special issue entitled 'Mobility and trafficking of neuronal membrane proteins'.
中文翻译:

KCC2膜扩散可调节神经元氯化物的稳态。
神经元Cl-稳态受两个阳离子氯化物共转运蛋白(CCC),K + -Cl-共同转运蛋白KCC2和Na + -K + -Cl-协同转运蛋白NKCC1的活性调节,它们分别在神经元中挤压和导入氯化物。几种神经和精神疾病,包括癫痫,神经性疼痛,精神分裂症和自闭症,都与神经元氯化物(Cl-)稳态的改变有关。当前的观点是,由于KCC2下调和/或NKCC1上调而导致的神经元内细胞内Cl-的积累可能会削弱抑制性GABA信号传导,从而促进病理活动的发展。CCC活性主要取决于它们在质膜中的表达水平。此外,CCC在膜中会发生“扩散捕获”,通过依赖于活性的翻译后修饰,即关键丝氨酸和苏氨酸残基的磷酸化/去磷酸化,可以快速调节该机制。这可能是使CCC功能适应神经元活动变化的最快速的细胞机制。因此,在病理情况下干扰这些机制可能有助于恢复Cl稳态和抑制作用。本文是题为“神经元膜蛋白的移动性和运输”的特刊的一部分。干扰这些机制可能有助于恢复Cl-稳态和在病理条件下的抑制作用。本文是题为“神经元膜蛋白的移动性和运输”的特刊的一部分。干扰这些机制可能有助于恢复Cl-稳态和在病理条件下的抑制作用。本文是题为“神经元膜蛋白的移动性和运输”的特刊的一部分。
更新日期:2019-12-13
中文翻译:

KCC2膜扩散可调节神经元氯化物的稳态。
神经元Cl-稳态受两个阳离子氯化物共转运蛋白(CCC),K + -Cl-共同转运蛋白KCC2和Na + -K + -Cl-协同转运蛋白NKCC1的活性调节,它们分别在神经元中挤压和导入氯化物。几种神经和精神疾病,包括癫痫,神经性疼痛,精神分裂症和自闭症,都与神经元氯化物(Cl-)稳态的改变有关。当前的观点是,由于KCC2下调和/或NKCC1上调而导致的神经元内细胞内Cl-的积累可能会削弱抑制性GABA信号传导,从而促进病理活动的发展。CCC活性主要取决于它们在质膜中的表达水平。此外,CCC在膜中会发生“扩散捕获”,通过依赖于活性的翻译后修饰,即关键丝氨酸和苏氨酸残基的磷酸化/去磷酸化,可以快速调节该机制。这可能是使CCC功能适应神经元活动变化的最快速的细胞机制。因此,在病理情况下干扰这些机制可能有助于恢复Cl稳态和抑制作用。本文是题为“神经元膜蛋白的移动性和运输”的特刊的一部分。干扰这些机制可能有助于恢复Cl-稳态和在病理条件下的抑制作用。本文是题为“神经元膜蛋白的移动性和运输”的特刊的一部分。干扰这些机制可能有助于恢复Cl-稳态和在病理条件下的抑制作用。本文是题为“神经元膜蛋白的移动性和运输”的特刊的一部分。






























 京公网安备 11010802027423号
京公网安备 11010802027423号