当前位置:
X-MOL 学术
›
ACS Appl. Mater. Interfaces
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
基于近红外光响应性二硫化钼纳米片的药物输送系统可控制地塞米松的高效释放,从而抑制炎症和治疗骨关节炎
ACS Applied Materials & Interfaces ( IF 8.3 ) Pub Date : 2019-03-07 00:00:00 , DOI: 10.1021/acsami.8b20372 Yingyu Zhao 1 , Chunfang Wei 1 , Xu Chen 1 , Jiawei Liu 1 , Qianqian Yu 1 , Yanan Liu 1 , Jie Liu 1
ACS Applied Materials & Interfaces ( IF 8.3 ) Pub Date : 2019-03-07 00:00:00 , DOI: 10.1021/acsami.8b20372 Yingyu Zhao 1 , Chunfang Wei 1 , Xu Chen 1 , Jiawei Liu 1 , Qianqian Yu 1 , Yanan Liu 1 , Jie Liu 1
Affiliation
|
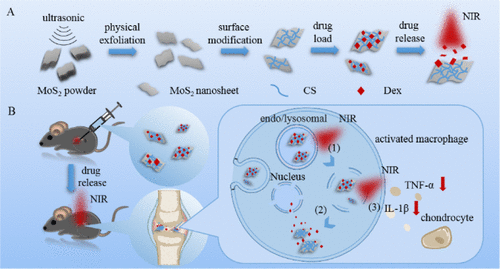
关节腔内注射在治疗骨关节炎(OA)方面具有独特的优势,尽管它可能会迅速清除关节腔内的治疗药物。将治疗剂与功能化的纳米载体结合可以提供有效的解决方案。通过载药纳米系统控制关节腔内药物的治疗浓度可以协同治疗OA。在这里,我们提出了一种使用壳聚糖(CS)修饰的二硫化钼(MoS 2)的关节内药物递送纳米系统MoS 2 @ [电子邮件保护](MCD)。纳米片作为近红外(NIR)光响应载体,并装有抗炎药地塞米松(Dex)。MCD在体内和体外均对NIR光有反应,并通过光热转化触发Dex释放。这样可以通过调节NIR光的辐射行为,在关节腔中进行遥控的Dex释放。MCD延长了Dex在关节腔中的停留时间。关节腔内注射MCD和NIR辐射可确保低全身剂量Dex的治疗效果显着提高,从而减轻OA中由TNF-α和IL-1β等炎性因子分泌引起的软骨侵蚀。体内新陈代谢过程中对其他内部器官的毒性和副作用有所减少。此外,MoS的光声成像能力2个纳米片用于检测关节腔中MCD的代谢。我们的研究表明,MCD具有治疗OA的巨大潜力。

"点击查看英文标题和摘要"
更新日期:2019-03-07

"点击查看英文标题和摘要"































 京公网安备 11010802027423号
京公网安备 11010802027423号