当前位置:
X-MOL 学术
›
J. Am. Chem. Soc.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Nanoscale ATP-responsive Zeolitic Imidazole Framework-90 as a General Platform for Cytosolic Protein Delivery and Genome Editing
Journal of the American Chemical Society ( IF 14.4 ) Pub Date : 2019-02-06 , DOI: 10.1021/jacs.8b11996 Xiaoti Yang 1, 2 , Qiao Tang 1, 3 , Ying Jiang 1 , Meining Zhang 3 , Ming Wang 1, 2 , Lanqun Mao 1, 2
Journal of the American Chemical Society ( IF 14.4 ) Pub Date : 2019-02-06 , DOI: 10.1021/jacs.8b11996 Xiaoti Yang 1, 2 , Qiao Tang 1, 3 , Ying Jiang 1 , Meining Zhang 3 , Ming Wang 1, 2 , Lanqun Mao 1, 2
Affiliation
|
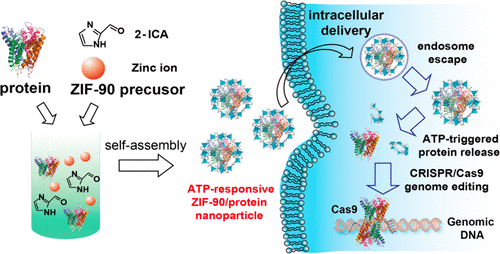
Metal-organic frameworks (MOFs) are an emerging class of nanocarriers for drug delivery, owing to their tunable chemical functionality. Here we report ATP-responsive zeolitic imidazole framework-90 (ZIF-90) as a general platform for cytosolic protein delivery and CRISPR/Cas9 genome editing. The self-assembly of imidazole-2-carboxaldehyde and Zn2+ with protein forms ZIF-90/protein nanoparticles and efficiently encapsulates protein. It was found that, in the presence of ATP, the ZIF-90/protein nanoparticles are degraded to release protein due to the competitive coordination between ATP and the Zn2+ of ZIF-90. Intracellular delivery studies showed that the ZIF-90/protein nanoparticle can deliver a large variety of proteins into the cytosol, regardless of protein size and molecular weight. The delivery of cytotoxic RNase A efficiently prohibits tumor cell growth, while the effective delivery of genome-editing protein Cas9 knocks out the green fluorescent protein (GFP) expression of HeLa cells with efficiency up to 35%. Given the fact that ATP is upregulated in disease cells, it is envisaged that the ATP-responsive protein delivery will open up new opportunities for an advanced protein delivery and CRISPR/Cas9 genome editing for targeted disease treatment.
中文翻译:

纳米级 ATP 响应沸石咪唑框架 90 作为细胞溶质蛋白传递和基因组编辑的通用平台
金属有机框架 (MOF) 是一类新兴的用于药物递送的纳米载体,因为它们具有可调的化学功能。在这里,我们报告了 ATP 响应性沸石咪唑框架 90 (ZIF-90) 作为细胞溶质蛋白递送和 CRISPR/Cas9 基因组编辑的通用平台。咪唑-2-甲醛和Zn2+与蛋白质的自组装形成ZIF-90/蛋白质纳米颗粒并有效地封装蛋白质。研究发现,在 ATP 存在下,由于 ATP 与 ZIF-90 的 Zn2+ 之间的竞争配位,ZIF-90/蛋白质纳米颗粒降解释放蛋白质。细胞内递送研究表明,无论蛋白质大小和分子量如何,ZIF-90/蛋白质纳米颗粒都可以将多种蛋白质递送到细胞质中。细胞毒性 RNase A 的传递有效地抑制了肿瘤细胞的生长,而基因组编辑蛋白 Cas9 的有效传递以高达 35% 的效率敲除 HeLa 细胞的绿色荧光蛋白 (GFP) 表达。鉴于 ATP 在疾病细胞中上调这一事实,预计 ATP 响应性蛋白质递送将为高级蛋白质递送和用于靶向疾病治疗的 CRISPR/Cas9 基因组编辑开辟新的机会。
更新日期:2019-02-06
中文翻译:

纳米级 ATP 响应沸石咪唑框架 90 作为细胞溶质蛋白传递和基因组编辑的通用平台
金属有机框架 (MOF) 是一类新兴的用于药物递送的纳米载体,因为它们具有可调的化学功能。在这里,我们报告了 ATP 响应性沸石咪唑框架 90 (ZIF-90) 作为细胞溶质蛋白递送和 CRISPR/Cas9 基因组编辑的通用平台。咪唑-2-甲醛和Zn2+与蛋白质的自组装形成ZIF-90/蛋白质纳米颗粒并有效地封装蛋白质。研究发现,在 ATP 存在下,由于 ATP 与 ZIF-90 的 Zn2+ 之间的竞争配位,ZIF-90/蛋白质纳米颗粒降解释放蛋白质。细胞内递送研究表明,无论蛋白质大小和分子量如何,ZIF-90/蛋白质纳米颗粒都可以将多种蛋白质递送到细胞质中。细胞毒性 RNase A 的传递有效地抑制了肿瘤细胞的生长,而基因组编辑蛋白 Cas9 的有效传递以高达 35% 的效率敲除 HeLa 细胞的绿色荧光蛋白 (GFP) 表达。鉴于 ATP 在疾病细胞中上调这一事实,预计 ATP 响应性蛋白质递送将为高级蛋白质递送和用于靶向疾病治疗的 CRISPR/Cas9 基因组编辑开辟新的机会。


















































 京公网安备 11010802027423号
京公网安备 11010802027423号