当前位置:
X-MOL 学术
›
Biomaterials
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
使用肽缀合的超小纳米药物载体双重靶向Wnt和uPA受体抑制了耐化学性乳腺癌中的癌症干细胞表型
Biomaterials ( IF 12.8 ) Pub Date : 2017-10-21 , DOI: 10.1016/j.biomaterials.2017.10.035 Jasmine Miller-Kleinhenz , Xiangxue Guo , Weiping Qian , Hongyu Zhou , Erica N. Bozeman , Lei Zhu , Xin Ji , Y.Andrew Wang , Toncred Styblo , Ruth O'Regan , Hui Mao , Lily Yang
Biomaterials ( IF 12.8 ) Pub Date : 2017-10-21 , DOI: 10.1016/j.biomaterials.2017.10.035 Jasmine Miller-Kleinhenz , Xiangxue Guo , Weiping Qian , Hongyu Zhou , Erica N. Bozeman , Lei Zhu , Xin Ji , Y.Andrew Wang , Toncred Styblo , Ruth O'Regan , Hui Mao , Lily Yang
|
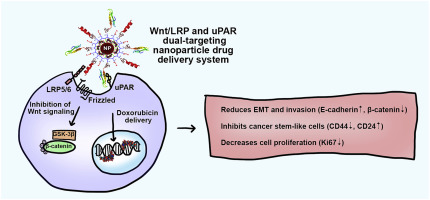
异质性肿瘤细胞,肿瘤复发的高发生率和总体存活率的下降是化学耐药性乳腺癌治疗的主要挑战。我们的研究结果显示,在同一患者中建立的乳腺癌患者异种移植(PDX)肿瘤之间存在不同的化学治疗反应。相对于对Dox敏感的肿瘤,所有对阿霉素(Dox)耐药的肿瘤均表达较高水平的癌症干样细胞生物标志物,包括CD44,Wnt及其受体LRP5 / 6。为了有效治疗抗药性肿瘤,我们开发了一种超小型磁性氧化铁纳米粒子(IONP)药物载体,该载体与双重靶向Wnt / LRP5 / 6和尿激酶纤溶酶原激活剂受体(uPAR)的肽缀合。我们的结果表明,需要双重受体靶向的IONPs与LRP5 / 6和uPAR同时结合才能抑制乳腺癌细胞的侵袭。分子分析表明,靶向双受体的IONPs显着抑制了肿瘤细胞的Wnt /β-catenin信号传导和癌干样表型,并显着降低了Wnt配体,CD44和uPAR。与人类乳腺癌PDX模型中的非靶向或单靶向IONP-Dox相比,双重靶向IONP的系统性给药导致将纳米颗粒药物递送到PDX肿瘤中,从而导致更强的肿瘤生长抑制作用。因此,使用IONP药物载体将Wnt / LRP和uPAR共同靶向是有效地将药物递送给耐化学性乳腺癌的有前途的治疗方法。分子分析表明,靶向双受体的IONPs显着抑制了肿瘤细胞的Wnt /β-catenin信号传导和癌干样表型,并显着降低了Wnt配体,CD44和uPAR。与人类乳腺癌PDX模型中的非靶向或单靶向IONP-Dox相比,双重靶向IONP的系统性给药导致将纳米颗粒药物递送到PDX肿瘤中,从而导致更强的肿瘤生长抑制作用。因此,使用IONP药物载体将Wnt / LRP和uPAR共同靶向是有效地将药物递送给耐化学性乳腺癌的有前途的治疗方法。分子分析表明,靶向双受体的IONPs显着抑制了肿瘤细胞的Wnt /β-catenin信号传导和癌干样表型,并显着降低了Wnt配体,CD44和uPAR。与人类乳腺癌PDX模型中的非靶向或单靶向IONP-Dox相比,双重靶向IONP的系统性给药导致将纳米颗粒药物递送到PDX肿瘤中,从而导致更强的肿瘤生长抑制作用。因此,使用IONP药物载体将Wnt / LRP和uPAR共同靶向是有效地将药物递送给耐化学性乳腺癌的有前途的治疗方法。与人类乳腺癌PDX模型中的非靶向或单靶向IONP-Dox相比,双重靶向IONP的全身给药导致将纳米颗粒药物递送到PDX肿瘤中,从而导致更强的肿瘤生长抑制作用。因此,使用IONP药物载体将Wnt / LRP和uPAR共同靶向是有效地将药物递送给耐化学性乳腺癌的有前途的治疗方法。与人类乳腺癌PDX模型中的非靶向或单靶向IONP-Dox相比,双重靶向IONP的系统性给药导致将纳米颗粒药物递送到PDX肿瘤中,从而导致更强的肿瘤生长抑制作用。因此,使用IONP药物载体将Wnt / LRP和uPAR共同靶向是有效地将药物递送给耐化学性乳腺癌的有前途的治疗方法。

"点击查看英文标题和摘要"
更新日期:2017-10-21

"点击查看英文标题和摘要"































 京公网安备 11010802027423号
京公网安备 11010802027423号