Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
禽呼肠孤病毒p17和σA通过抑制mTORC2和CDK2 / cyclin A2并上调蛋白酶体PSMB6协同作用来下调Akt。
Scientific Reports ( IF 3.8 ) Pub Date : 2017-07-12 , DOI: 10.1038/s41598-017-05510-x
Wei-Ru Huang , Pei-I Chi , Hung-Chuan Chiu , Jue-Liang Hsu , Brent L. Nielsen , Tsai-Ling Liao , Hung-Jen Liu
Scientific Reports ( IF 3.8 ) Pub Date : 2017-07-12 , DOI: 10.1038/s41598-017-05510-x
Wei-Ru Huang , Pei-I Chi , Hung-Chuan Chiu , Jue-Liang Hsu , Brent L. Nielsen , Tsai-Ling Liao , Hung-Jen Liu
|
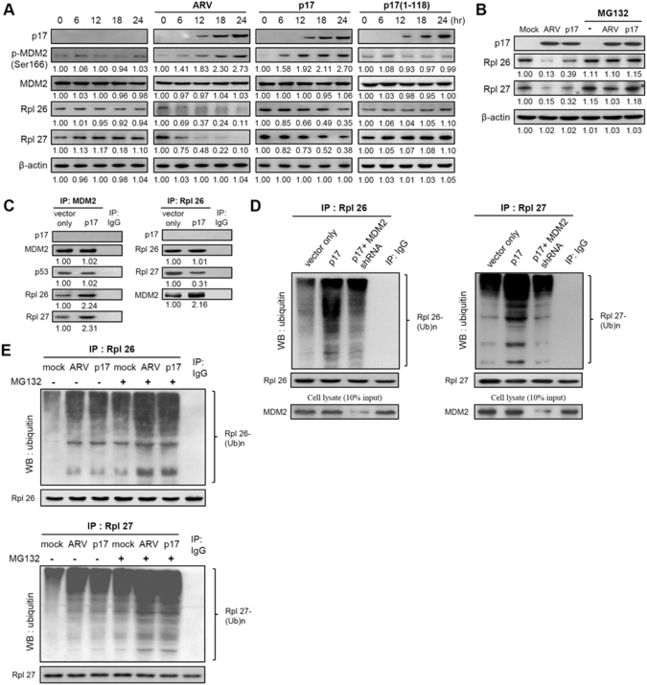
尽管我们已经表明禽呼肠孤病毒(ARV)p17介导的对Akt的抑制导致自噬的诱导,但是确切的机制在很大程度上仍然未知。这项研究已经确定了一种特殊的机制,通过该机制,ARV通过p17介导的靶向核糖体蛋白的E3连接酶MDM2的活化以及σA介导的蛋白酶体PSMB6的上调,来协调调节核糖体蛋白的降解。除了下调核糖体蛋白外,p17还减少了mTORC2的装配并破坏了mTORC2-robosome的结合,这两者都使mTORC2失活,从而导致S473处Akt磷酸化的抑制。此外,我们发现p17绑定并抑制CDK2 / cyclin A2复合物,进一步抑制Akt S473的磷酸化。在用胰岛素或CDK2过度表达处理的细胞中,p17对mTORC2组装和S473处Akt磷酸化的负面影响被逆转。p17的羧基末端对于与CDK2相互作用和诱导自噬是必需的。此外,p17介导的LC3-II的上调可以通过CDK2的过量表达而部分逆转。本研究提供了机制的见解,通过下调mTORC2和CDK2 / cyclin A2的复合物并上调PSMB6来抑制ARV的p17蛋白和σA蛋白之间的合作,从而对Akt产生负调控,从而共同诱导自噬和细胞周期停滞并有益于病毒复制。p17介导的LC3-II的上调可以通过CDK2的过量表达而部分逆转。本研究提供了机制的见解,通过下调mTORC2和CDK2 / cyclin A2的复合物并上调PSMB6来抑制ARV的p17蛋白和σA蛋白之间的合作,从而对Akt产生负调控,从而共同诱导自噬和细胞周期停滞并有益于病毒复制。p17介导的LC3-II的上调可以通过CDK2的过量表达而部分逆转。本研究提供了机制的见解,通过下调mTORC2和CDK2 / cyclin A2的复合物并上调PSMB6来抑制ARV的p17蛋白和σA蛋白之间的合作,从而对Akt产生负调控,从而共同诱导自噬和细胞周期停滞并有益于病毒复制。

"点击查看英文标题和摘要"
更新日期:2017-07-13

"点击查看英文标题和摘要"

































 京公网安备 11010802027423号
京公网安备 11010802027423号