当前位置:
X-MOL 学术
›
Nat. Commun.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
An L-threonine transaldolase is required for L-threo-β-hydroxy-α-amino acid assembly during obafluorin biosynthesis.
Nature Communications ( IF 14.7 ) Pub Date : 2017-06-26 , DOI: 10.1038/ncomms15935 Thomas A Scott 1 , Daniel Heine 1 , Zhiwei Qin 1 , Barrie Wilkinson 1
Nature Communications ( IF 14.7 ) Pub Date : 2017-06-26 , DOI: 10.1038/ncomms15935 Thomas A Scott 1 , Daniel Heine 1 , Zhiwei Qin 1 , Barrie Wilkinson 1
Affiliation
|
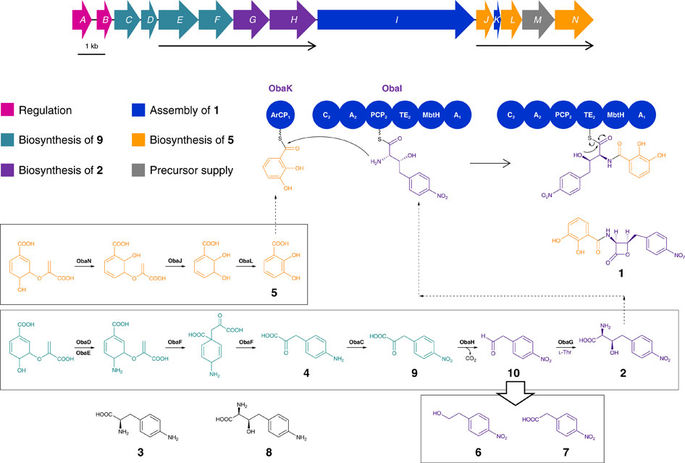
β-Lactone natural products occur infrequently in nature but possess a variety of potent and valuable biological activities. They are commonly derived from β-hydroxy-α-amino acids, which are themselves valuable chiral building blocks for chemical synthesis and precursors to numerous important medicines. However, despite a number of excellent synthetic methods for their asymmetric synthesis, few effective enzymatic tools exist for their preparation. Here we report cloning of the biosynthetic gene cluster for the β-lactone antibiotic obafluorin and delineate its biosynthetic pathway. We identify a nonribosomal peptide synthetase with an unusual domain architecture and an L-threonine:4-nitrophenylacetaldehyde transaldolase responsible for (2S,3R)-2-amino-3-hydroxy-4-(4-nitrophenyl)butanoate biosynthesis. Phylogenetic analysis sheds light on the evolutionary origin of this rare enzyme family and identifies further gene clusters encoding L-threonine transaldolases. We also present preliminary data suggesting that L-threonine transaldolases might be useful for the preparation of L-threo-β-hydroxy-α-amino acids.
中文翻译:

在奥巴氟林生物合成过程中,L-苏氨酸转醛醇酶是 L-苏氨酸-β-羟基-α-氨基酸组装所必需的。
β-内酯天然产物在自然界中很少出现,但具有多种有效且有价值的生物活性。它们通常衍生自 β-羟基-α-氨基酸,这些氨基酸本身就是化学合成中有价值的手性构件,也是许多重要药物的前体。然而,尽管有许多出色的不对称合成方法,但用于制备它们的有效酶促工具却很少。在这里,我们报道了β-内酯抗生素奥巴氟林生物合成基因簇的克隆,并描绘了其生物合成途径。我们鉴定了一种具有不寻常结构域结构的非核糖体肽合成酶和负责 (2S,3R)-2-氨基-3-羟基-4-(4-硝基苯基)丁酸生物合成的 L-苏氨酸:4-硝基苯乙醛转醛醇酶。系统发育分析揭示了这一罕见酶家族的进化起源,并进一步鉴定了编码 L-苏氨酸转醛醇酶的基因簇。我们还提供了初步数据,表明 L-苏氨酸转醛醇酶可能可用于制备 L-苏氨酸-β-羟基-α-氨基酸。
更新日期:2017-06-27
中文翻译:

在奥巴氟林生物合成过程中,L-苏氨酸转醛醇酶是 L-苏氨酸-β-羟基-α-氨基酸组装所必需的。
β-内酯天然产物在自然界中很少出现,但具有多种有效且有价值的生物活性。它们通常衍生自 β-羟基-α-氨基酸,这些氨基酸本身就是化学合成中有价值的手性构件,也是许多重要药物的前体。然而,尽管有许多出色的不对称合成方法,但用于制备它们的有效酶促工具却很少。在这里,我们报道了β-内酯抗生素奥巴氟林生物合成基因簇的克隆,并描绘了其生物合成途径。我们鉴定了一种具有不寻常结构域结构的非核糖体肽合成酶和负责 (2S,3R)-2-氨基-3-羟基-4-(4-硝基苯基)丁酸生物合成的 L-苏氨酸:4-硝基苯乙醛转醛醇酶。系统发育分析揭示了这一罕见酶家族的进化起源,并进一步鉴定了编码 L-苏氨酸转醛醇酶的基因簇。我们还提供了初步数据,表明 L-苏氨酸转醛醇酶可能可用于制备 L-苏氨酸-β-羟基-α-氨基酸。


















































 京公网安备 11010802027423号
京公网安备 11010802027423号