Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
细菌纳米囊泡作为介导疼痛超敏反应的界间信号部分
ACS Nano ( IF 15.8 ) Pub Date : 2025-01-16 , DOI: 10.1021/acsnano.4c10529
Sameh Almousa 1 , Susy Kim 1 , Ashish Kumar 1 , Yixin Su 1 , Sangeeta Singh 1 , Shalini Mishra 1 , Miriam M Fonseca 2 , Hilal A Rather 1 , E Alfonso Romero-Sandoval 2 , Fang-Chi Hsu 3, 4 , Rakesh Singh 5 , Hariom Yadav 6 , Santosh Mishra 7, 8 , Gagan Deep 1, 4, 9
Affiliation
|
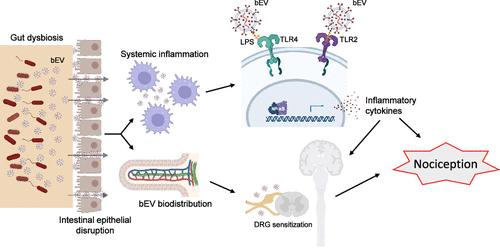
肠道菌群失调会导致多种病理,但肠道菌群介导的对全身和远处反应影响的机制在很大程度上仍然难以捉摸。本研究旨在确定纳米细菌细胞外囊泡 (bEV) 在饮食诱导的肥胖 (DIO) 肠道菌群失调模型中介导异常性疼痛,即疼痛超敏反应中的作用。通过结合超速离心和免疫沉淀的方法,从瘦 (bEVLean) 和 DIO (bEVDIO) 小鼠的粪便中富集 bEV,然后广泛分析纯度和细菌特性。接下来,在小鼠体内或静脉内注射 bEV 以评估疼痛敏感性。通过灌肠将荧光标记的 bEVs 注射到小鼠体内以评估生物分布。通过阵列、免疫表型分析、显微镜检查、NF-κB 活化和细胞摄取测定分析 bEV 对免疫细胞和炎症的影响。结果显示,在野生型小鼠中施用 bEVDIO 复制了在 DIO 小鼠中观察到的机械和热刺激异常性疼痛表型。重要的是,这种效果在 TRPA1/TRPV1 双重敲除小鼠中受到了影响。生物分布分析显示 bEV 进入体循环,随后定位在远处。多项分析表明,bEVDIO 暴露主要通过调节先天免疫系统引发全身炎症。这种炎症机制涉及 bEV 表面的 LPS,激活 TLR2 和 TLR4 相关通路,使用 TLR2 和 TLR4 抑制剂和剃除 bEV 表面蛋白证实了这一点。有趣的是,bEVDIO 的细胞摄取增强取决于涉及 LPS 和 bEV 上的蛋白质以及单核细胞上的 TLR2/TLR4 的相互作用。 这些发现阐明了 bEV 作为与肠道菌群失调相关的异常性疼痛和炎症的关键介质的作用,这是迄今为止未被探索的作用。

"点击查看英文标题和摘要"

































 京公网安备 11010802027423号
京公网安备 11010802027423号