当前位置:
X-MOL 学术
›
Environ. Pollut.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
6-PPD quinone causes lipid accumulation across multiple generations differentially affected by metabolic sensors and components of COMPASS complex in Caenorhabditis elegans
Environmental Pollution ( IF 7.6 ) Pub Date : 2024-12-15 , DOI: 10.1016/j.envpol.2024.125539 Yuxing Wang, Jingwei Wu, Dayong Wang
Environmental Pollution ( IF 7.6 ) Pub Date : 2024-12-15 , DOI: 10.1016/j.envpol.2024.125539 Yuxing Wang, Jingwei Wu, Dayong Wang
|
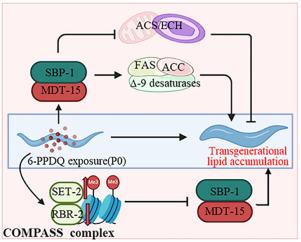
The toxicity of 6-PPD quinone (6-PPDQ) has been frequently detected. However, the possible transgenerational effects of 6-PPDQ remain largely unclear. Due to short life cycle and high sensitivity to environmental exposure, Caenorhabditis elegans is useful for study of transgenerational toxicology. In C. elegans , we observed the transgenerational increase in lipid accumulation after parental generation (P0-G) exposure to 6-PPDQ at 0.1–10 μg/L. Accompanied with this, transgenerational increase in expressions of genes governing fatty acid synthesis and monounsaturated fatty acyl-CoAs synthesis and decrease in genes governing fatty acid β-oxidation were induced by 6-PPDQ exposure. Moreover, 6-PPDQ exposure at P0-G caused transgenerational activation of mdt-15 and sbp-1 encoding lipid metabolic sensors. Meanwhile, exposure to 6-PPDQ induced transgenerational activation of set-2 and inhibition in rbr-2 , two genes encoding components of COMPASS complex. The 6-PPDQ induced transgenerational lipid accumulation could be strengthened by RNAi of set-2 and suppressed by RNAi of rbr-2 . Additionally, 6-PPDQ induced transgenerational neurotoxicity could be increased by RNAi of mdt-15 , sbp-1 , and rbr-2 , and inhibited by RNAi of set-2 . Therefore, our results demonstrated the possibility in resulting in transgenerational lipid accumulation by exposure to 6-PPDQ.
中文翻译:

6-PPD 醌导致多代脂质积累,受秀丽隐杆线虫中代谢传感器和 COMPASS 复合物成分的影响不同
6-PPD 醌 (6-PPDQ) 的毒性已经常被检测到。然而,6-PPDQ 可能的跨代影响在很大程度上仍不清楚。由于生命周期短且对环境暴露高度敏感,秀丽隐杆线虫可用于跨代毒理学研究。在秀丽隐杆线虫中,我们观察到亲代 (P0-G) 暴露于 0.1-10 μg/L 的 6-PPDQ 后脂质积累的跨代增加。与此同时,6-PPDQ 暴露诱导了控制脂肪酸合成和单不饱和脂肪酰基辅酶 A 合成的基因表达的跨代增加以及控制脂肪酸β-氧化的基因的减少。此外,P0-G 的 6-PPDQ 暴露导致编码脂质代谢传感器的 mdt-15 和 sbp-1 的跨代激活。同时,暴露于 6-PPDQ 诱导 set-2 的跨代激活和 rbr-2 的抑制,这两个基因编码 COMPASS 复合物的成分。set-2 的 RNAi 可加强 6-PPDQ 诱导的跨反代脂质积累,而 rbr-2 的 RNAi 可抑制 6-PPDQ 诱导的跨反代脂质积累。此外,mdt-15 、 sbp-1 和 rbr-2 的 RNAi 可增加 6-PPDQ 诱导的跨代神经毒性,而 set-2 的 RNAi 可抑制 6-PPDQ 诱导的跨代神经毒性。因此,我们的结果表明了暴露于 6-PPDQ 导致跨代脂质积累的可能性。
更新日期:2024-12-15
中文翻译:

6-PPD 醌导致多代脂质积累,受秀丽隐杆线虫中代谢传感器和 COMPASS 复合物成分的影响不同
6-PPD 醌 (6-PPDQ) 的毒性已经常被检测到。然而,6-PPDQ 可能的跨代影响在很大程度上仍不清楚。由于生命周期短且对环境暴露高度敏感,秀丽隐杆线虫可用于跨代毒理学研究。在秀丽隐杆线虫中,我们观察到亲代 (P0-G) 暴露于 0.1-10 μg/L 的 6-PPDQ 后脂质积累的跨代增加。与此同时,6-PPDQ 暴露诱导了控制脂肪酸合成和单不饱和脂肪酰基辅酶 A 合成的基因表达的跨代增加以及控制脂肪酸β-氧化的基因的减少。此外,P0-G 的 6-PPDQ 暴露导致编码脂质代谢传感器的 mdt-15 和 sbp-1 的跨代激活。同时,暴露于 6-PPDQ 诱导 set-2 的跨代激活和 rbr-2 的抑制,这两个基因编码 COMPASS 复合物的成分。set-2 的 RNAi 可加强 6-PPDQ 诱导的跨反代脂质积累,而 rbr-2 的 RNAi 可抑制 6-PPDQ 诱导的跨反代脂质积累。此外,mdt-15 、 sbp-1 和 rbr-2 的 RNAi 可增加 6-PPDQ 诱导的跨代神经毒性,而 set-2 的 RNAi 可抑制 6-PPDQ 诱导的跨代神经毒性。因此,我们的结果表明了暴露于 6-PPDQ 导致跨代脂质积累的可能性。






























 京公网安备 11010802027423号
京公网安备 11010802027423号