Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Phase separation of chimeric antigen receptor promotes immunological synapse maturation and persistent cytotoxicity
Immunity ( IF 25.5 ) Pub Date : 2024-11-27 , DOI: 10.1016/j.immuni.2024.11.005 Xinyi Xu, Haotian Chen, Zhengxu Ren, Xiaomin Xu, Wei Wu, Haochen Yang, JinJiao Wang, Yumeng Zhang, Qiuping Zhou, Hua Li, Shaoqing Zhang, Haopeng Wang, Chenqi Xu
Immunity ( IF 25.5 ) Pub Date : 2024-11-27 , DOI: 10.1016/j.immuni.2024.11.005 Xinyi Xu, Haotian Chen, Zhengxu Ren, Xiaomin Xu, Wei Wu, Haochen Yang, JinJiao Wang, Yumeng Zhang, Qiuping Zhou, Hua Li, Shaoqing Zhang, Haopeng Wang, Chenqi Xu
|
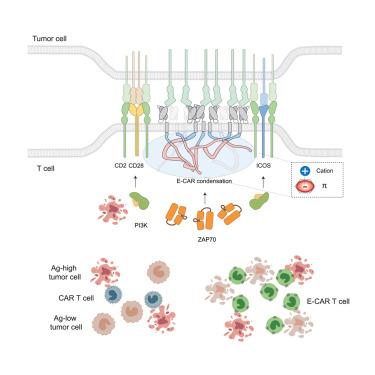
Major challenges of chimeric antigen receptor (CAR)-T cell therapy include poor antigen sensitivity and cell persistence. Here, we report a solution to these issues by exploiting CAR phase separation. We found that incorporation of an engineered T cell receptor CD3ε motif, EB6I , into the conventional 28Z or BBZ CAR induced self-phase separation through cation-π interactions. EB6I CAR formed a mature immunological synapse with the CD2 corolla to transduce efficient antigen and costimulatory signaling, although its tonic signaling remained low. Functionally, EB6I CAR-T cells exhibited improved signaling and cytotoxicity against low-antigen tumor cells and persistent tumor-killing function. In multiple primary and relapsed murine tumor models, EB6I CAR-T cells exerted better antitumor functions than conventional CAR-T cells against blood and solid cancers. This study thus unveils a CAR engineering strategy to improve CAR-T cell immunity by leveraging molecular condensation and signaling integration.
中文翻译:

嵌合抗原受体的相分离促进免疫突触成熟和持续的细胞毒性
嵌合抗原受体 (CAR)-T 细胞疗法的主要挑战包括抗原敏感性差和细胞持久性。在这里,我们报告了通过利用 CAR 相分离来解决这些问题的方法。我们发现,将工程化的 T 细胞受体 CD3ε 基序 EB6I 掺入传统的 28Z 或 BBZ CAR 中,通过阳离子-π相互作用诱导自相分离。EB6I CAR 与 CD2 花冠形成成熟的免疫突触,以转导有效的抗原和共刺激信号传导,但其强直信号传导仍然很低。在功能上,EB6I CAR-T 细胞对低抗原肿瘤细胞表现出改进的信号传导和细胞毒性以及持续的肿瘤杀伤功能。在多个原发性和复发性小鼠肿瘤模型中,EB6I CAR-T 细胞比常规 CAR-T 细胞对血液癌和实体癌发挥了更好的抗肿瘤功能。因此,本研究揭示了一种 CAR 工程策略,通过利用分子凝聚和信号传导整合来提高 CAR-T 细胞免疫力。
更新日期:2024-11-27
中文翻译:

嵌合抗原受体的相分离促进免疫突触成熟和持续的细胞毒性
嵌合抗原受体 (CAR)-T 细胞疗法的主要挑战包括抗原敏感性差和细胞持久性。在这里,我们报告了通过利用 CAR 相分离来解决这些问题的方法。我们发现,将工程化的 T 细胞受体 CD3ε 基序 EB6I 掺入传统的 28Z 或 BBZ CAR 中,通过阳离子-π相互作用诱导自相分离。EB6I CAR 与 CD2 花冠形成成熟的免疫突触,以转导有效的抗原和共刺激信号传导,但其强直信号传导仍然很低。在功能上,EB6I CAR-T 细胞对低抗原肿瘤细胞表现出改进的信号传导和细胞毒性以及持续的肿瘤杀伤功能。在多个原发性和复发性小鼠肿瘤模型中,EB6I CAR-T 细胞比常规 CAR-T 细胞对血液癌和实体癌发挥了更好的抗肿瘤功能。因此,本研究揭示了一种 CAR 工程策略,通过利用分子凝聚和信号传导整合来提高 CAR-T 细胞免疫力。

































 京公网安备 11010802027423号
京公网安备 11010802027423号