当前位置:
X-MOL 学术
›
Anal. Chem.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Enzyme-Free Identification of Monosaccharide Enantiomers on TiO2 Nanotube Array-Based Fabry–Pérot Interferometer
Analytical Chemistry ( IF 6.7 ) Pub Date : 2024-11-19 , DOI: 10.1021/acs.analchem.4c04160 Hairihan Zhou, Junli Guo, Zirui Wang, Junjian Zhao, Zhida Gao, Pei Song, Yan-Yan Song, Chenxi Zhao
Analytical Chemistry ( IF 6.7 ) Pub Date : 2024-11-19 , DOI: 10.1021/acs.analchem.4c04160 Hairihan Zhou, Junli Guo, Zirui Wang, Junjian Zhao, Zhida Gao, Pei Song, Yan-Yan Song, Chenxi Zhao
|
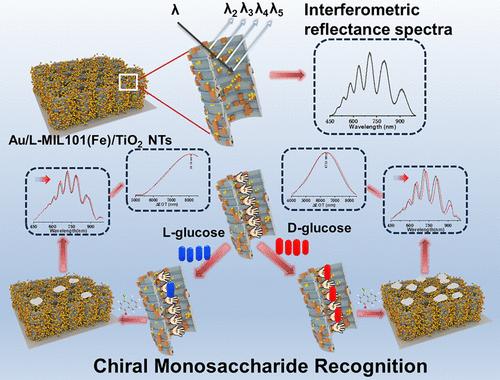
Chirality is a vital property across various domains, especially for biological activity. Herein, an enzyme-free sensing platform for monosaccharide enantiomer identification was developed by utilizing the Fabry–Pérot interferometer feature of TiO2 nanotube arrays modified with enantioselective metal–organic framework and glucose oxidase-mimicking Au NPs. In this design, optical property is monitored by reflective interferometric Fourier transform spectroscopy (RIFTS), a highly sensitive technique for detecting changes in the average refractive index within nanotubular structures. Using glucose (Glu) enantiomers as the model targets, after the recognition of L-/d-Glu on mesoporous homochiral MIL-101 (Fe), Au NPs anchored in MIL-101(Fe) catalyze the oxidation of Glu molecules to produce hydrogen peroxide (H2O2). Benefiting from the confinement effect of frameworks, MIL-101(Fe), as an artificial enzyme with excellent peroxidase-like activity, catalyzes the conversion of 4-chloro-1-naphthol (4-CN) into insoluble precipitates. These gathered precipitates effectively change the average refractive index of the interferometric substrate. Based on the variation of effective optical thickness (ΔEOT) values, the enantioselective determination of l-Glu and d-Glu can be achieved. Moreover, the proposed RIFTS sensor also presents broad applicability for the identification of other monosaccharide enantiomers. As the enzyme-free homochiral interferometer is directly constructed on a Ti-metal sheet, the RIFTS platform offers a robust, sensitive, and low-cost device for monosaccharide enantiomer recognition.
中文翻译:

在基于 TiO2 纳米管阵列的 Fabry-Pérot 干涉仪上无酶鉴定单糖对映异构体
手性是各个领域的重要特性,尤其是对于生物活性。在此,利用对映选择性金属有机框架和葡萄糖氧化酶模拟 Au NPs 修饰的 TiO2 纳米管阵列的 Fabry-Pérot 干涉仪功能,开发了一种用于单糖对映异构体鉴定的无酶传感平台。在本设计中,光学特性通过反射干涉傅里叶变换光谱 (RIFTS) 进行监测,RIFTS 是一种用于检测纳米管结构内平均折射率变化的高灵敏度技术。以葡萄糖 (Glu) 对映异构体为模型靶点,在介孔同手性 MIL-101 (Fe) 上识别 L-/d-Glu 后,锚定在 MIL-101(Fe) 中的 Au NPs 催化 Glu 分子氧化产生过氧化氢 (H2O2)。受益于框架的约束作用,MIL-101(Fe) 作为一种具有优异过氧化物酶样活性的人工酶,催化 4-氯-1-萘酚 (4-CN) 转化为不溶性沉淀物。这些聚集的沉淀物有效地改变了干涉基底的平均折射率。基于有效光学厚度 (ΔEOT) 值的变化,可以实现 l-Glu 和 d-Glu 的对映选择性测定。此外,所提出的 RIFTS 传感器还为识别其他单糖对映异构体提供了广泛的适用性。由于无酶同手性干涉仪直接构建在 Ti 金属板上,因此 RIFTS 平台为单糖对映异构体识别提供了一种稳健、灵敏且低成本的设备。
更新日期:2024-11-20
中文翻译:

在基于 TiO2 纳米管阵列的 Fabry-Pérot 干涉仪上无酶鉴定单糖对映异构体
手性是各个领域的重要特性,尤其是对于生物活性。在此,利用对映选择性金属有机框架和葡萄糖氧化酶模拟 Au NPs 修饰的 TiO2 纳米管阵列的 Fabry-Pérot 干涉仪功能,开发了一种用于单糖对映异构体鉴定的无酶传感平台。在本设计中,光学特性通过反射干涉傅里叶变换光谱 (RIFTS) 进行监测,RIFTS 是一种用于检测纳米管结构内平均折射率变化的高灵敏度技术。以葡萄糖 (Glu) 对映异构体为模型靶点,在介孔同手性 MIL-101 (Fe) 上识别 L-/d-Glu 后,锚定在 MIL-101(Fe) 中的 Au NPs 催化 Glu 分子氧化产生过氧化氢 (H2O2)。受益于框架的约束作用,MIL-101(Fe) 作为一种具有优异过氧化物酶样活性的人工酶,催化 4-氯-1-萘酚 (4-CN) 转化为不溶性沉淀物。这些聚集的沉淀物有效地改变了干涉基底的平均折射率。基于有效光学厚度 (ΔEOT) 值的变化,可以实现 l-Glu 和 d-Glu 的对映选择性测定。此外,所提出的 RIFTS 传感器还为识别其他单糖对映异构体提供了广泛的适用性。由于无酶同手性干涉仪直接构建在 Ti 金属板上,因此 RIFTS 平台为单糖对映异构体识别提供了一种稳健、灵敏且低成本的设备。


















































 京公网安备 11010802027423号
京公网安备 11010802027423号