Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Nanobiohybrid Extracellular Vesicle Nanoreactor with Improving Metabolical Activity for Biocatalytic Therapy
ACS Nano ( IF 15.8 ) Pub Date : 2024-11-13 , DOI: 10.1021/acsnano.4c12458 Shuangshuang Wan, Wurui Liu, Qian Wu, Kepeng Wang, Yaocheng Li, Peihong Huang, Yu Wu, Yunfei Mu, Yulin Fan, Jun Tao, Jia Yao, Fei Peng, Yu Zou, Lianhui Wang, Zhiyao Yuan, Xianguang Ding
ACS Nano ( IF 15.8 ) Pub Date : 2024-11-13 , DOI: 10.1021/acsnano.4c12458 Shuangshuang Wan, Wurui Liu, Qian Wu, Kepeng Wang, Yaocheng Li, Peihong Huang, Yu Wu, Yunfei Mu, Yulin Fan, Jun Tao, Jia Yao, Fei Peng, Yu Zou, Lianhui Wang, Zhiyao Yuan, Xianguang Ding
|
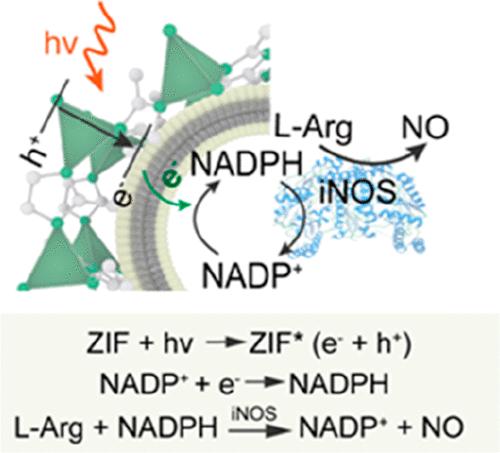
Extracellular vesicles (EVs) hosting enzymatic activities that function as independent metabolic units are attractive natural biocatalytic platforms. However, directly using these metabolically active nanoreactors for effective biocatalytic applications remains challenging, mainly due to their constrained catalytic capabilities. Here, we construct an EV-templated nanobiohybrid system by engineering an EV surface with a photoresponsive zeolitic imidazolate framework (ZIF). The deposition of ZIF nanostructures on EVs not only contributes to improved biocatalytic stability but also enables interfacial coupling between photoexcited electrons from the ZIF and the enzymatic reaction of metabolically active EVs. Nearly 300% of biomass conversion efficiency increment could be achieved by EVs derived from macrophages. This enhanced biocatalysis, high catalytic stability, and low cytotoxicity endowed the EV@ZIF nanosystem with robust biosynthesis and antimicrobial activity. When evaluated in a mouse periodontitis model, we show that the autologous biocatalytic EV@ZIF demonstrated efficient therapeutic capability by killing bacteria and inhibiting inflammation. This nanoengineering strategy will benefit the future optimization of metabolically active EV nanoreactors as biocatalysts for a broad range of therapeutics.
中文翻译:

用于生物催化治疗的纳米生物杂交细胞外囊泡纳米反应器,具有更高的代谢活性
承载酶活性的细胞外囊泡 (EV) 作为独立的代谢单位发挥作用,是有吸引力的天然生物催化平台。然而,直接使用这些代谢活性纳米反应器进行有效的生物催化应用仍然具有挑战性,这主要是由于它们的催化能力受到限制。在这里,我们通过使用光响应沸石咪唑框架 (ZIF) 设计 EV 表面来构建一个 EV 模板化的纳米生物混合系统。ZIF 纳米结构在 EV 上的沉积不仅有助于提高生物催化稳定性,而且还使来自 ZIF 的光激发电子与代谢活性 EV 的酶促反应之间的界面耦合成为可能。来自巨噬细胞的 EV 可以实现近 300% 的生物质转化效率提升。这种增强的生物催化、高催化稳定性和低细胞毒性赋予了 EV@ZIF 纳米系统强大的生物合成和抗菌活性。在小鼠牙周炎模型中进行评估时,我们表明自体生物催化EV@ZIF通过杀死细菌和抑制炎症表现出有效的治疗能力。这种纳米工程策略将有助于未来优化代谢活性的 EV 纳米反应器作为广泛治疗药物的生物催化剂。
更新日期:2024-11-14
中文翻译:

用于生物催化治疗的纳米生物杂交细胞外囊泡纳米反应器,具有更高的代谢活性
承载酶活性的细胞外囊泡 (EV) 作为独立的代谢单位发挥作用,是有吸引力的天然生物催化平台。然而,直接使用这些代谢活性纳米反应器进行有效的生物催化应用仍然具有挑战性,这主要是由于它们的催化能力受到限制。在这里,我们通过使用光响应沸石咪唑框架 (ZIF) 设计 EV 表面来构建一个 EV 模板化的纳米生物混合系统。ZIF 纳米结构在 EV 上的沉积不仅有助于提高生物催化稳定性,而且还使来自 ZIF 的光激发电子与代谢活性 EV 的酶促反应之间的界面耦合成为可能。来自巨噬细胞的 EV 可以实现近 300% 的生物质转化效率提升。这种增强的生物催化、高催化稳定性和低细胞毒性赋予了 EV@ZIF 纳米系统强大的生物合成和抗菌活性。在小鼠牙周炎模型中进行评估时,我们表明自体生物催化EV@ZIF通过杀死细菌和抑制炎症表现出有效的治疗能力。这种纳米工程策略将有助于未来优化代谢活性的 EV 纳米反应器作为广泛治疗药物的生物催化剂。


















































 京公网安备 11010802027423号
京公网安备 11010802027423号