Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
The development of a method to produce diagnostic reagents using LaNiO3 nanospheres and their application in nanozyme-linked immunosorbent assay for the colorimetric screening of C-reactive protein with high sensitivity
Analyst ( IF 3.6 ) Pub Date : 2024-10-21 , DOI: 10.1039/d4an01160k Maria Nikitina, Pavel Khramtsov, Stepan Devyatov, Rishat Valeev, Marina Eryomina, Andrey Chukavin, Mikhail Rayev
Analyst ( IF 3.6 ) Pub Date : 2024-10-21 , DOI: 10.1039/d4an01160k Maria Nikitina, Pavel Khramtsov, Stepan Devyatov, Rishat Valeev, Marina Eryomina, Andrey Chukavin, Mikhail Rayev
|
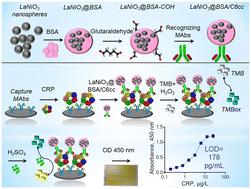
LaNiO3 perovskite nanoparticles, especially nanospheres (LNNS), show great promise in biomedical assays due to their peroxidase-like catalytic properties. However, LNNS-based diagnostic reagents have not been tested in nanozyme enzyme-linked immunosorbent assay (NLISA) or other enzyme-linked immunosorbent assays, and there is limited data on their synthesis. To fill this gap, it is necessary to develop a method for creating LNNS conjugates with monoclonal antibodies and to investigate the reproducibility, scalability, and applicability of these diagnostic reagents in NLISA. We have successfully developed a method for producing novel diagnostic reagents utilizing LaNiO3 nanospheres. Our research demonstrates the application of these nanospheres in a NLISA specifically designed for the detection of C-reactive protein (CRP) in real serum samples. This method is both reproducible and scalable, allowing for the efficient production of nanospheres that are functionalized with monoclonal antibodies targeting CRP, with a mean diameter of approximately 270 nm. Based on the promising results obtained from our experiments, we have developed and optimized a sandwich-format NLISA for CRP detection. This assay achieved a lower limit of detection at 0.178 μg L−1, with a dynamic range from 12.5 to 0.195 μg L−1 and a linear detection range extending from 0.195 to 6.25 μg L−1, showcasing its potential for clinical applications. The new NLISA method, utilizing LaNiO3 nanospheres in a sandwich format for the detection of CRP, significantly enhances sensitivity compared to similar use horseradish peroxidase-based ELISA. In this study for the first time, the functionalization of lanthanum nickelate nanospheres with recognition elements has been demonstrated. This advancement also sheds light on the technological challenges involved in synthesizing diagnostic reagents, identifying areas that need further exploration.
中文翻译:

利用 LaNiO3 纳米球生产诊断试剂的方法的开发及其在纳米酶连接免疫吸附测定中的应用,用于高灵敏度 C 反应蛋白的比色筛选
LaNiO3 钙钛矿纳米颗粒,尤其是纳米球 (LNNS),由于其类似过氧化物酶的催化特性,在生物医学测定中显示出巨大的前景。然而,基于 LNNS 的诊断试剂尚未在纳米酶联免疫吸附测定 (NLISA) 或其他酶联免疫吸附测定中进行测试,并且关于其合成的数据有限。为了填补这一空白,有必要开发一种使用单克隆抗体制备 LNNS 偶联物的方法,并研究这些诊断试剂在 NLISA 中的重现性、可扩展性和适用性。我们成功开发了一种利用 LaNiO3 纳米球生产新型诊断试剂的方法。我们的研究表明了这些纳米球在专门设计用于检测真实血清样品中 C 反应蛋白 (CRP) 的 NLISA 中的应用。这种方法既可重复又可扩展,可以高效生产用靶向 CRP 的单克隆抗体功能化的纳米球,平均直径约为 270 nm。基于我们从实验中获得的有希望的结果,我们开发并优化了用于 CRP 检测的夹心格式 NLISA。该测定的检测下限为 0.178 μg L-1,动态范围为 12.5 至 0.195 μg L-1,线性检测范围为 0.195 至 6.25 μg L-1,展示了其临床应用潜力。新的 NLISA 方法利用夹心形式的 LaNiO3 纳米球检测 CRP,与类似用途的基于辣根过氧化物酶的 ELISA 相比,显著提高了灵敏度。 在这项研究中,首次证明了具有识别元件的镍酸镧纳米球的功能化。这一进步还揭示了合成诊断试剂所涉及的技术挑战,确定了需要进一步探索的领域。
更新日期:2024-10-21
中文翻译:

利用 LaNiO3 纳米球生产诊断试剂的方法的开发及其在纳米酶连接免疫吸附测定中的应用,用于高灵敏度 C 反应蛋白的比色筛选
LaNiO3 钙钛矿纳米颗粒,尤其是纳米球 (LNNS),由于其类似过氧化物酶的催化特性,在生物医学测定中显示出巨大的前景。然而,基于 LNNS 的诊断试剂尚未在纳米酶联免疫吸附测定 (NLISA) 或其他酶联免疫吸附测定中进行测试,并且关于其合成的数据有限。为了填补这一空白,有必要开发一种使用单克隆抗体制备 LNNS 偶联物的方法,并研究这些诊断试剂在 NLISA 中的重现性、可扩展性和适用性。我们成功开发了一种利用 LaNiO3 纳米球生产新型诊断试剂的方法。我们的研究表明了这些纳米球在专门设计用于检测真实血清样品中 C 反应蛋白 (CRP) 的 NLISA 中的应用。这种方法既可重复又可扩展,可以高效生产用靶向 CRP 的单克隆抗体功能化的纳米球,平均直径约为 270 nm。基于我们从实验中获得的有希望的结果,我们开发并优化了用于 CRP 检测的夹心格式 NLISA。该测定的检测下限为 0.178 μg L-1,动态范围为 12.5 至 0.195 μg L-1,线性检测范围为 0.195 至 6.25 μg L-1,展示了其临床应用潜力。新的 NLISA 方法利用夹心形式的 LaNiO3 纳米球检测 CRP,与类似用途的基于辣根过氧化物酶的 ELISA 相比,显著提高了灵敏度。 在这项研究中,首次证明了具有识别元件的镍酸镧纳米球的功能化。这一进步还揭示了合成诊断试剂所涉及的技术挑战,确定了需要进一步探索的领域。


















































 京公网安备 11010802027423号
京公网安备 11010802027423号