当前位置:
X-MOL 学术
›
Chem. Sci.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Acylhydrazone-based reversibly photoswitchable ion pair transporter with OFF–ON cotransport activity
Chemical Science ( IF 7.6 ) Pub Date : 2024-08-30 , DOI: 10.1039/d4sc02474e Sandip Chattopadhayay , Paras Wanjari , Pinaki Talukdar
Chemical Science ( IF 7.6 ) Pub Date : 2024-08-30 , DOI: 10.1039/d4sc02474e Sandip Chattopadhayay , Paras Wanjari , Pinaki Talukdar
|
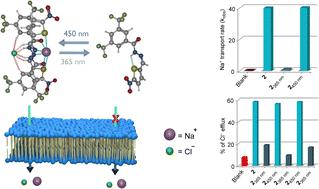
The cellular membrane transport of physiologically important cations and anions is omnipresent and regulates different physiological functions. Whereas a notable number of cation–anion transporters are being developed to transport salts across the membrane, developing an artificial cation–anion symporter with stimulus-responsive activities is an immense obstacle. Herein, for the first time, we report reversibly photoswitchable acylhydrazone-based transporter 2 that has distinctive OFF–ON cation–anion co-transport abilities. The substituent was modified in 1a–1c and 2, to change the to-and-fro movement of the transporter to enhance the ion transport efficiency. Ion transport experiments across the lipid bilayer membrane demonstrate that 1a has the highest transport activity among the series with irreversible photoisomerization properties, whereas 2 has a unique reversible photoisomerization property. A detailed transport study indicated that the E-conformer of compound 2 facilitates Na+/Cl− transport via the symport process by following the carrier mode of ion transport. 23Na NMR and chloride selective electrode assays confirmed the OFF and ON state of ion transport of compound 2 with photoirradiation. An assembly of [(2E)2 + NaCl] was subjected to geometry optimization to understand the responsible ion binding motif. Geometry optimization followed by the natural bond orbital analysis of 1aZ and 2Z demonstrated that 1aZ forms comparatively stronger intramolecular H-bonding than 2Z, making it accessible for reversible photoisomerization.
中文翻译:

基于酰基腙的可逆光开关离子对转运蛋白,具有 OFF-ON 共转运活性
生理上重要的阳离子和阴离子的细胞膜转运无处不在,并调节不同的生理功能。虽然正在开发大量阳离子-阴离子转运蛋白来跨膜运输盐,但开发具有刺激反应活性的人工阳离子-阴离子同向转运蛋白是一个巨大的障碍。在此,我们首次报道了可逆的基于酰腙的可逆光开关转运蛋白 2,它具有独特的 OFF-ON 阳离子-阴离子共转运能力。取代基在 1a–1c 和 2 中被修饰,以改变转运蛋白的来回运动,从而提高离子传输效率。跨脂质双层膜的离子传输实验表明,在具有不可逆光异构化特性的系列中,1a 具有最高的传输活性,而 2 具有独特的可逆光异构化特性。一项详细的传输研究表明,化合物 2 的 E-构象异构体通过遵循离子传输的载体模式,通过同向端口过程促进 Na + / Cl− 传输。23Na NMR 和氯化物选择性电极测定证实了化合物 2 在光照射下离子传输的 OFF 和 ON 状态。对 [(2E)2 + NaCl] 的组装体进行几何优化,以了解负责的离子结合基序。 几何优化后对 1aZ 和 2Z 进行自然键轨道分析,表明 1aZ 形成的分子内 H 键比 2Z 强,使其可用于可逆光异构化。
更新日期:2024-08-30
中文翻译:

基于酰基腙的可逆光开关离子对转运蛋白,具有 OFF-ON 共转运活性
生理上重要的阳离子和阴离子的细胞膜转运无处不在,并调节不同的生理功能。虽然正在开发大量阳离子-阴离子转运蛋白来跨膜运输盐,但开发具有刺激反应活性的人工阳离子-阴离子同向转运蛋白是一个巨大的障碍。在此,我们首次报道了可逆的基于酰腙的可逆光开关转运蛋白 2,它具有独特的 OFF-ON 阳离子-阴离子共转运能力。取代基在 1a–1c 和 2 中被修饰,以改变转运蛋白的来回运动,从而提高离子传输效率。跨脂质双层膜的离子传输实验表明,在具有不可逆光异构化特性的系列中,1a 具有最高的传输活性,而 2 具有独特的可逆光异构化特性。一项详细的传输研究表明,化合物 2 的 E-构象异构体通过遵循离子传输的载体模式,通过同向端口过程促进 Na + / Cl− 传输。23Na NMR 和氯化物选择性电极测定证实了化合物 2 在光照射下离子传输的 OFF 和 ON 状态。对 [(2E)2 + NaCl] 的组装体进行几何优化,以了解负责的离子结合基序。 几何优化后对 1aZ 和 2Z 进行自然键轨道分析,表明 1aZ 形成的分子内 H 键比 2Z 强,使其可用于可逆光异构化。

































 京公网安备 11010802027423号
京公网安备 11010802027423号