Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
B(C6F5)3-catalyzed selective C–H chalcogenation of arenes and heteroarenes
Chem ( IF 19.1 ) Pub Date : 2024-06-27 , DOI: 10.1016/j.chempr.2024.05.025
Milan Pramanik , Sampurna Das , Rasool Babaahmadi , Sanjukta Pahar , Thomas Wirth , Emma Richards , Rebecca L. Melen
Chem ( IF 19.1 ) Pub Date : 2024-06-27 , DOI: 10.1016/j.chempr.2024.05.025
Milan Pramanik , Sampurna Das , Rasool Babaahmadi , Sanjukta Pahar , Thomas Wirth , Emma Richards , Rebecca L. Melen
|
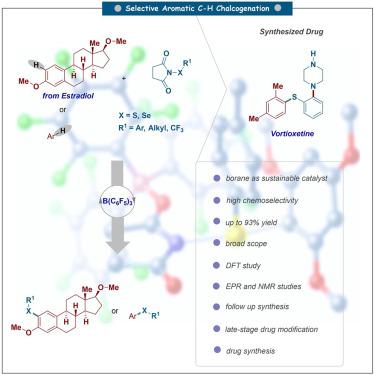
The synthesis of organochalcogenides remains a valuable area of research due to their widespread biological applications, particularly in pharmaceuticals. Herein, our study details the B(C6 F5 )3 -catalyzed Csp2 –H functionalization of diverse arenes, heteroarenes, and pharmacophores with thiosuccinimides or selenosuccinimides, providing selective access to chalcogenated products. This protocol enables the selective late-stage chalcogenation of drug molecules such as the anti-inflammatory drug naproxen, the estrogen steroid hormone estradiol derivatives, and the industrially relevant trifluoromethylthiolation reaction. Furthermore, this C–S coupling methodology provides a facile and metal-free route to synthesize vortioxetine, an antidepressant drug, and a plethora of significant organic motifs. Detailed NMR, EPR analyses, and density functional theory (DFT) computational studies indicate that the elongation of the thiosuccinimide N–S bond is assisted by a boron-centered adduct, which then leads to a stable ion pair with an arene. The EPR analysis shows that a transient radical pair, potentially an off-cycle species, is not directly involved in the catalytic process.
中文翻译:

B(C6F5)3 催化芳烃和杂芳烃的选择性 C-H 硫属化反应
由于其广泛的生物应用,特别是在制药领域,有机硫属化物的合成仍然是一个有价值的研究领域。在此,我们的研究详细介绍了 B(C6F5)3 催化的各种芳烃、杂芳烃和药效团与硫代琥珀酰亚胺或硒代琥珀酰亚胺的 Csp2-H 官能化,提供了选择性获得硫属产品的方法。该方案能够选择性地对药物分子进行后期硫属化,例如抗炎药萘普生、雌激素类固醇激素雌二醇衍生物以及工业相关的三氟甲基硫基化反应。此外,这种 C-S 偶联方法提供了一种简便且无金属的路线来合成沃替西汀(一种抗抑郁药物)和大量重要的有机基序。详细的 NMR、EPR 分析和密度泛函理论 (DFT) 计算研究表明,硫代琥珀酰亚胺 N-S 键的伸长得到硼中心加合物的帮助,然后与芳烃形成稳定的离子对。 EPR 分析表明,瞬态自由基对(可能是非循环物质)不直接参与催化过程。
更新日期:2024-06-27
中文翻译:

B(C6F5)3 催化芳烃和杂芳烃的选择性 C-H 硫属化反应
由于其广泛的生物应用,特别是在制药领域,有机硫属化物的合成仍然是一个有价值的研究领域。在此,我们的研究详细介绍了 B(C6F5)3 催化的各种芳烃、杂芳烃和药效团与硫代琥珀酰亚胺或硒代琥珀酰亚胺的 Csp2-H 官能化,提供了选择性获得硫属产品的方法。该方案能够选择性地对药物分子进行后期硫属化,例如抗炎药萘普生、雌激素类固醇激素雌二醇衍生物以及工业相关的三氟甲基硫基化反应。此外,这种 C-S 偶联方法提供了一种简便且无金属的路线来合成沃替西汀(一种抗抑郁药物)和大量重要的有机基序。详细的 NMR、EPR 分析和密度泛函理论 (DFT) 计算研究表明,硫代琥珀酰亚胺 N-S 键的伸长得到硼中心加合物的帮助,然后与芳烃形成稳定的离子对。 EPR 分析表明,瞬态自由基对(可能是非循环物质)不直接参与催化过程。

































 京公网安备 11010802027423号
京公网安备 11010802027423号