当前位置:
X-MOL 学术
›
RSC Med. Chem.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Computational design, synthesis, and assessment of 3-(4-(4-(1,3,4-oxadiazol-2-yl)-1H-imidazol-2-yl)phenyl)-1,2,4-oxadiazole derivatives as effective epidermal growth factor receptor inhibitors: a prospective strategy for anticancer therapy
RSC Medicinal Chemistry ( IF 4.1 ) Pub Date : 2024-04-11 , DOI: 10.1039/d4md00055b Nilesh Raghunath Khedkar 1 , Milind Sindkhedkar 1 , Alex Joseph 2
RSC Medicinal Chemistry ( IF 4.1 ) Pub Date : 2024-04-11 , DOI: 10.1039/d4md00055b Nilesh Raghunath Khedkar 1 , Milind Sindkhedkar 1 , Alex Joseph 2
Affiliation
|
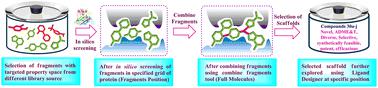
The epidermal growth factor receptor (EGFR) enzyme plays a critical role in governing the cell cycle, positioning it as a promising target for the development of anticancer drugs. In this study, we endeavored to design and synthesize innovative EGFR inhibitors with potential applications in anticancer therapy. A novel series of compounds, namely 3-(4-(4-(1,3,4-oxadiazol-2-yl)-1H-imidazol-2-yl)phenyl)-1,2,4-oxadiazoles (30a–j), were meticulously designed using FBDD efforts and synthesized. The synthesized compounds underwent thorough characterization using 1HNMR, 13CNMR, HRMS, and mass spectrum analyses. The in vitro anticancer activities of the newly developed compounds (30a–j) were evaluated against four human cancer cell lines such as prostate cancer (PC3 & DU-145), lung cancer (A549), and liver cancer (HEPG2) using the MTT method. The results, expressed as IC50 values, demonstrated significant anticancer activity for several compounds, with five compounds (30a, 30b, 30c, 30i, and 30j) exhibiting superior potency compared to the established anticancer drug etoposide. Notably, compound 30a emerged as the most promising compound, displaying potent cytotoxicity. We also conducted a screening of the compounds on the normal Vero cell line, revealing a pronounced selectivity of the compounds against cancer cell lines, with no observable impact on the normal cell lines. Moreover, the synthesized compounds were investigated for their impact on enzyme EGFR activity. The findings revealed a robust inhibitory effect against the EGFR wild-type enzyme and a 10-fold inferior potency against the mutant form of EGFR. This observation underscores the potential of the new derivatives as effective EGFRWT inhibitors with substantial anticancer efficacy. Further studies, including cell cycle analysis and apoptosis assays in HEPG2 cell lines, revealed cell cycle arrest at G1/G0 and G2 phases. We also evaluated the potential influence of compound 30a on the EGFR pathway using western blot analysis, revealing a significant inhibition of EGFR autophosphorylation in HEPG2 cells. In conclusion, our findings highlight the promise of these novel compounds as potent EGFR inhibitors, encouraging further investigation and development for the creation of novel and effective anticancer therapeutics.
中文翻译:

3-(4-(4-(1,3,4-恶二唑-2-基)-1H-咪唑-2-基)苯基)-1,2,4-恶二唑衍生物作为有效的表皮生长因子受体抑制剂的计算设计、合成和评估:抗癌治疗的前瞻性策略
表皮生长因子受体 (EGFR) 酶在控制细胞周期中起着关键作用,使其成为抗癌药物开发的有前途的靶点。在这项研究中,我们努力设计和合成具有抗癌治疗潜在应用的创新 EGFR 抑制剂。使用 FBDD 努力精心设计并合成了一系列新型化合物,即 3-(4-(4-(1,3,4-恶唑-2-基)-1H-咪唑-2-基)苯基)-1,2,4-恶二唑 (30a-j)。使用 1个 HNMR、13个 CNMR、HRMS 和质谱分析对合成的化合物进行了全面的表征。使用MTT方法评估了新开发的化合物(30a-j)对四种人类癌细胞系的体外抗癌活性,如前列腺癌(PC3和DU-145),肺癌(A549)和肝癌(HEPG2)。以 IC50 值表示的结果显示,对几种化合物具有显着的抗癌活性,其中五种化合物(30a、30b、30c、30i 和 30j)与已建立的抗癌药物依托泊苷相比表现出优异的效力。值得注意的是,化合物 30a 成为最有前途的化合物,显示出强大的细胞毒性。我们还在正常 Vero 细胞系上对化合物进行了筛选,揭示了这些化合物对癌细胞系的显着选择性,对正常细胞系没有明显的影响。此外,研究了合成化合物对酶 EGFR 活性的影响。研究结果显示,对 EGFR 野生型酶具有强大的抑制作用,而对 EGFR 突变形式的效力低 10 倍。 这一观察结果强调了新衍生物作为有效的 EGFRWT 抑制剂的潜力,具有显着的抗癌功效。进一步的研究,包括 HEPG2 细胞系中的细胞周期分析和细胞凋亡测定,揭示了细胞周期停滞在 G1/G0 和 G2 期。我们还使用 western blot 分析评估了化合物 30a 对 EGFR 通路的潜在影响,揭示了 HEPG2 细胞中 EGFR 自磷酸化的显着抑制。总之,我们的研究结果强调了这些新化合物作为有效的 EGFR 抑制剂的前景,鼓励进一步研究和开发以创造新颖有效的抗癌疗法。
更新日期:2024-04-12
中文翻译:

3-(4-(4-(1,3,4-恶二唑-2-基)-1H-咪唑-2-基)苯基)-1,2,4-恶二唑衍生物作为有效的表皮生长因子受体抑制剂的计算设计、合成和评估:抗癌治疗的前瞻性策略
表皮生长因子受体 (EGFR) 酶在控制细胞周期中起着关键作用,使其成为抗癌药物开发的有前途的靶点。在这项研究中,我们努力设计和合成具有抗癌治疗潜在应用的创新 EGFR 抑制剂。使用 FBDD 努力精心设计并合成了一系列新型化合物,即 3-(4-(4-(1,3,4-恶唑-2-基)-1H-咪唑-2-基)苯基)-1,2,4-恶二唑 (30a-j)。使用 1个 HNMR、13个 CNMR、HRMS 和质谱分析对合成的化合物进行了全面的表征。使用MTT方法评估了新开发的化合物(30a-j)对四种人类癌细胞系的体外抗癌活性,如前列腺癌(PC3和DU-145),肺癌(A549)和肝癌(HEPG2)。以 IC50 值表示的结果显示,对几种化合物具有显着的抗癌活性,其中五种化合物(30a、30b、30c、30i 和 30j)与已建立的抗癌药物依托泊苷相比表现出优异的效力。值得注意的是,化合物 30a 成为最有前途的化合物,显示出强大的细胞毒性。我们还在正常 Vero 细胞系上对化合物进行了筛选,揭示了这些化合物对癌细胞系的显着选择性,对正常细胞系没有明显的影响。此外,研究了合成化合物对酶 EGFR 活性的影响。研究结果显示,对 EGFR 野生型酶具有强大的抑制作用,而对 EGFR 突变形式的效力低 10 倍。 这一观察结果强调了新衍生物作为有效的 EGFRWT 抑制剂的潜力,具有显着的抗癌功效。进一步的研究,包括 HEPG2 细胞系中的细胞周期分析和细胞凋亡测定,揭示了细胞周期停滞在 G1/G0 和 G2 期。我们还使用 western blot 分析评估了化合物 30a 对 EGFR 通路的潜在影响,揭示了 HEPG2 细胞中 EGFR 自磷酸化的显着抑制。总之,我们的研究结果强调了这些新化合物作为有效的 EGFR 抑制剂的前景,鼓励进一步研究和开发以创造新颖有效的抗癌疗法。






























 京公网安备 11010802027423号
京公网安备 11010802027423号