当前位置:
X-MOL 学术
›
ACS Appl. Bio Mater.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Design and Construction of a Multi-Tiered Minimal Actin Cortex for Structural Support in Lipid Bilayer Applications
ACS Applied Bio Materials ( IF 4.6 ) Pub Date : 2024-03-01 , DOI: 10.1021/acsabm.3c01267 Amanda J Smith 1 , Theodore R B Larsen 1 , Harmony K Zimmerman 1 , Samuel J Virolainen 1 , Joshua J Meyer 1 , Lisa M Keranen Burden 1 , Daniel L Burden 1
ACS Applied Bio Materials ( IF 4.6 ) Pub Date : 2024-03-01 , DOI: 10.1021/acsabm.3c01267 Amanda J Smith 1 , Theodore R B Larsen 1 , Harmony K Zimmerman 1 , Samuel J Virolainen 1 , Joshua J Meyer 1 , Lisa M Keranen Burden 1 , Daniel L Burden 1
Affiliation
|
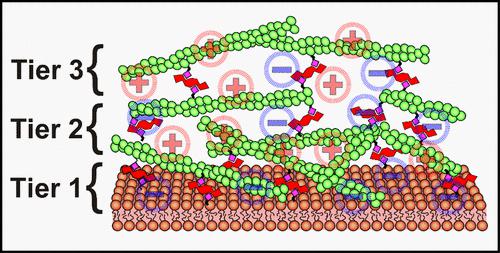
Artificial lipid bilayers have revolutionized biochemical and biophysical research by providing a versatile interface to study aspects of cell membranes and membrane-bound processes in a controlled environment. Artificial bilayers also play a central role in numerous biosensing applications, form the foundational interface for liposomal drug delivery, and provide a vital structure for the development of synthetic cells. But unlike the envelope in many living cells, artificial bilayers can be mechanically fragile. Here, we develop prototype scaffolds for artificial bilayers made from multiple chemically linked tiers of actin filaments that can be bonded to lipid headgroups. We call the interlinked and layered assembly a multiple minimal actin cortex (multi-MAC). Construction of multi-MACs has the potential to significantly increase the bilayer’s resistance to applied stress while retaining many desirable physical and chemical properties that are characteristic of lipid bilayers. Furthermore, the linking chemistry of multi-MACs is generalizable and can be applied almost anywhere lipid bilayers are important. This work describes a filament-by-filament approach to multi-MAC assembly that produces distinct 2D and 3D architectures. The nature of the structure depends on a combination of the underlying chemical conditions. Using fluorescence imaging techniques in model planar bilayers, we explore how multi-MACs vary with electrostatic charge, assembly time, ionic strength, and type of chemical linker. We also assess how the presence of a multi-MAC alters the underlying lateral diffusion of lipids and investigate the ability of multi-MACs to withstand exposure to shear stress.
中文翻译:

多层最小肌动蛋白皮层的设计和构建,用于脂质双层应用中的结构支持
人工脂质双层通过提供通用接口来研究受控环境中的细胞膜和膜结合过程的各个方面,彻底改变了生物化学和生物物理研究。人工双层还在众多生物传感应用中发挥着核心作用,形成脂质体药物输送的基础界面,并为合成细胞的发育提供重要的结构。但与许多活细胞的包膜不同,人造双层在机械上可能很脆弱。在这里,我们开发了由多层化学连接的肌动蛋白丝制成的人工双层原型支架,这些肌动蛋白丝可以与脂质头基结合。我们将这种相互连接的分层组件称为多重最小肌动蛋白皮层(multi-MAC)。多 MAC 的构建有可能显着提高双层对施加压力的抵抗力,同时保留脂质双层特征的许多理想的物理和化学性质。此外,多 MAC 的连接化学是可推广的,几乎可以应用于任何重要的脂质双层。这项工作描述了一种逐根细丝的多 MAC 组装方法,可产生不同的 2D 和 3D 架构。结构的性质取决于基础化学条件的组合。利用平面双层模型中的荧光成像技术,我们探索了多 MAC 如何随静电荷、组装时间、离子强度和化学连接体类型的变化而变化。我们还评估了 multi-MAC 的存在如何改变脂质的潜在横向扩散,并研究了 multi-MAC 承受剪切应力的能力。
更新日期:2024-03-01
中文翻译:

多层最小肌动蛋白皮层的设计和构建,用于脂质双层应用中的结构支持
人工脂质双层通过提供通用接口来研究受控环境中的细胞膜和膜结合过程的各个方面,彻底改变了生物化学和生物物理研究。人工双层还在众多生物传感应用中发挥着核心作用,形成脂质体药物输送的基础界面,并为合成细胞的发育提供重要的结构。但与许多活细胞的包膜不同,人造双层在机械上可能很脆弱。在这里,我们开发了由多层化学连接的肌动蛋白丝制成的人工双层原型支架,这些肌动蛋白丝可以与脂质头基结合。我们将这种相互连接的分层组件称为多重最小肌动蛋白皮层(multi-MAC)。多 MAC 的构建有可能显着提高双层对施加压力的抵抗力,同时保留脂质双层特征的许多理想的物理和化学性质。此外,多 MAC 的连接化学是可推广的,几乎可以应用于任何重要的脂质双层。这项工作描述了一种逐根细丝的多 MAC 组装方法,可产生不同的 2D 和 3D 架构。结构的性质取决于基础化学条件的组合。利用平面双层模型中的荧光成像技术,我们探索了多 MAC 如何随静电荷、组装时间、离子强度和化学连接体类型的变化而变化。我们还评估了 multi-MAC 的存在如何改变脂质的潜在横向扩散,并研究了 multi-MAC 承受剪切应力的能力。































 京公网安备 11010802027423号
京公网安备 11010802027423号