当前位置:
X-MOL 学术
›
Am. J. Hematol.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Safety and long-term survival results of the addition of inotuzumab ozogamicin to the conditioning regimen of allogeneic stem cell transplantation: A single-center phase 1,2 trial
American Journal of Hematology ( IF 10.1 ) Pub Date : 2024-02-23 , DOI: 10.1002/ajh.27254
Issa F Khouri 1 , Kamal Alzahrani 1 , Hagop Kantarjian 2 , Denái R Milton 3 , Alison M Gulbis 4 , Koji Sasaki 2 , Nitin Jain 2 , Nicholas J Short 2 , Tapan Kadia 2 , May Daher 1 , Hind Rafei 1 , Jin S Im 1 , David Marin 1 , Amanda L Olson 1 , Uday Popat 1 , Muzaffar Qazilbash 1 , Jeremy Ramdial 1 , Gabriela Rondon 1 , Samer Srour 1 , Partow Kebriaei 1 , Elizabeth Shpall 1 , Richard Champlin 1 , Elias J Jabbour 2
American Journal of Hematology ( IF 10.1 ) Pub Date : 2024-02-23 , DOI: 10.1002/ajh.27254
Issa F Khouri 1 , Kamal Alzahrani 1 , Hagop Kantarjian 2 , Denái R Milton 3 , Alison M Gulbis 4 , Koji Sasaki 2 , Nitin Jain 2 , Nicholas J Short 2 , Tapan Kadia 2 , May Daher 1 , Hind Rafei 1 , Jin S Im 1 , David Marin 1 , Amanda L Olson 1 , Uday Popat 1 , Muzaffar Qazilbash 1 , Jeremy Ramdial 1 , Gabriela Rondon 1 , Samer Srour 1 , Partow Kebriaei 1 , Elizabeth Shpall 1 , Richard Champlin 1 , Elias J Jabbour 2
Affiliation
|
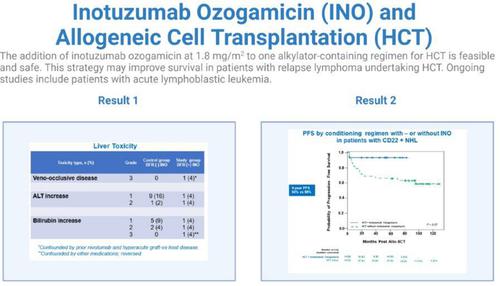
Here we report on the first prospective study evaluating the safety and long-term survival when an escalating dose of inotuzumab ozogamicin (INO) (0.6, 1.2, or 1.8 mg/m2 on day 13) was added to one alkylator-containing conditioning regimen in patients with relapsed CD22 (+) lymphoid malignancies who were candidates for hematopoietic stem cell transplantation (HSCT). Twenty-six patients were enrolled. Six (23%) of these patients entered the phase 1 study: four were treated at an INO dose of 0.6 mg/m2 and two at dose of 1.2 mg/m2. None of these patients experienced dose-limiting toxicities. The remaining 20 (77%) patients entered the phase 2 part of the study at the maximum dose of 1.8 mg/m2. One patient developed VOD; this patient had received nivolumab immediately before HSCT while simultaneously experiencing hyperacute graft-vs-host disease (GVHD). Treatment-related mortality (TRM) at 5 years was 12%. With a median follow-up of 48.7 months, the 5-year overall survival (OS) and progression-free survival (PFS) rates were 84% and 80%, respectively. Compared with a historical cohort who received same conditioning for HSCT but without INO (n = 56), the INO group showed no significant differences in incidence of liver toxicity, engraftment time, TRM, or risk of acute GVHD. Patients with lymphoma who received INO had a trend for a better 5-year OS (93% versus 68%) and PFS (93% versus 58%) than those in the control group. In conclusion, our results showed that INO is safe with no increased risk of VOD when combined with one alkylator-containing regimen of HSCT.
中文翻译:

在同种异体干细胞移植的预处理方案中添加伊珠单抗奥佐米星的安全性和长期生存结果:单中心1,2期试验
在此,我们报告了第一项前瞻性研究,该研究评估了将递增剂量的伊珠单抗奥佐米星 (INO)(第 13 天为 0.6、1.2 或 1.8 mg/m 2 )添加到含烷化剂的预处理方案中时的安全性和长期生存率适合接受造血干细胞移植 (HSCT) 的复发性 CD22 (+) 淋巴恶性肿瘤患者。共有 26 名患者入组。这些患者中有 6 名 (23%) 进入了 1 期研究:4 名患者接受 0.6 mg/m 2的 INO 剂量治疗,2 名患者接受 1.2 mg/m 2剂量的 INO 治疗。这些患者均未出现剂量限制性毒性。其余20名(77%)患者以最大剂量1.8 mg/m 2进入研究的2期部分。一名患者出现 VOD;该患者在 HSCT 前立即接受了纳武单抗治疗,同时患有超急性移植物抗宿主病 (GVHD)。 5 年治疗相关死亡率 (TRM) 为 12%。中位随访时间为 48.7 个月,5 年总生存率 (OS) 和无进展生存率 (PFS) 分别为 84% 和 80%。与接受相同 HSCT 预处理但不使用 INO 的历史队列( n = 56)相比,INO 组在肝毒性发生率、移植时间、TRM 或急性 GVHD 风险方面没有显着差异。接受 INO 治疗的淋巴瘤患者的 5 年 OS(93% 对 68%)和 PFS(93% 对 58%)比对照组患者有更好的趋势。总之,我们的结果表明,INO 与一种含有烷化剂的 HSCT 方案联合使用时是安全的,不会增加 VOD 风险。
更新日期:2024-02-23
中文翻译:

在同种异体干细胞移植的预处理方案中添加伊珠单抗奥佐米星的安全性和长期生存结果:单中心1,2期试验
在此,我们报告了第一项前瞻性研究,该研究评估了将递增剂量的伊珠单抗奥佐米星 (INO)(第 13 天为 0.6、1.2 或 1.8 mg/m 2 )添加到含烷化剂的预处理方案中时的安全性和长期生存率适合接受造血干细胞移植 (HSCT) 的复发性 CD22 (+) 淋巴恶性肿瘤患者。共有 26 名患者入组。这些患者中有 6 名 (23%) 进入了 1 期研究:4 名患者接受 0.6 mg/m 2的 INO 剂量治疗,2 名患者接受 1.2 mg/m 2剂量的 INO 治疗。这些患者均未出现剂量限制性毒性。其余20名(77%)患者以最大剂量1.8 mg/m 2进入研究的2期部分。一名患者出现 VOD;该患者在 HSCT 前立即接受了纳武单抗治疗,同时患有超急性移植物抗宿主病 (GVHD)。 5 年治疗相关死亡率 (TRM) 为 12%。中位随访时间为 48.7 个月,5 年总生存率 (OS) 和无进展生存率 (PFS) 分别为 84% 和 80%。与接受相同 HSCT 预处理但不使用 INO 的历史队列( n = 56)相比,INO 组在肝毒性发生率、移植时间、TRM 或急性 GVHD 风险方面没有显着差异。接受 INO 治疗的淋巴瘤患者的 5 年 OS(93% 对 68%)和 PFS(93% 对 58%)比对照组患者有更好的趋势。总之,我们的结果表明,INO 与一种含有烷化剂的 HSCT 方案联合使用时是安全的,不会增加 VOD 风险。

































 京公网安备 11010802027423号
京公网安备 11010802027423号