Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
通过分子伴侣介导的嵌合纳米平台自噬靶向降解信号转导和转录激活剂 3
ACS Nano ( IF 15.8 ) Pub Date : 2023-12-29 , DOI: 10.1021/acsnano.3c09536 Haohao Song 1, 2 , Wenping Huang 1, 3 , Fuhao Jia 1, 3 , Zhihang Wang 1, 3 , Jie Zhang 1, 3 , Ruihao Qian 1, 3 , Gungjun Nie 1, 3 , Hai Wang 1, 3
Affiliation
|
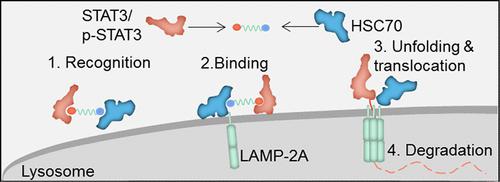
分子伴侣介导的自噬(CMA)是一种溶酶体依赖性蛋白水解途径,用于降解胞浆蛋白。然而,利用 CMA 介导的蛋白水解来降解癌症治疗中感兴趣的蛋白质尚未得到广泛应用。在这项研究中,我们开发了一种 CMA 靶向嵌合体 (CMATAC),可有效且特异性地降解肿瘤细胞中的信号转导和转录激活剂 3 (STAT3)。 CMATAC 由通过接头连接的 STAT3 和热休克同源 70 kDa 蛋白 (HSC70) 靶向肽组成。为了有效地将CMATAC递送至肿瘤细胞内,采用脂质纳米粒子(LNP)封装CMATAC(nCMATAC),并用胰岛素样生长因子2受体(IGF2R)靶向肽(InCMATAC)修饰,以实现肿瘤靶向和精确递送。模拟禁食饮食 (FMD) 可激活肿瘤细胞中的 CMA 通路。此外,FMD 治疗通过上调 IGF2R 表达,强烈增强 InCMATAC 的细胞摄取和肿瘤积累。因此,InCMATAC 可以有效降解 A549 和 HCC827 肿瘤细胞中的 STAT3 蛋白,并抑制体内肿瘤生长。这项研究表明 InCMATAC 可用于癌症治疗中的选择性蛋白水解。

"点击查看英文标题和摘要"































 京公网安备 11010802027423号
京公网安备 11010802027423号