当前位置:
X-MOL 学术
›
Adv. Funct. Mater.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
基于多功能介孔聚多巴胺的 STING 激动剂系统递送用于增强协同光热免疫治疗
Advanced Functional Materials ( IF 18.5 ) Pub Date : 2023-09-15 , DOI: 10.1002/adfm.202307241 Wenfeng Zeng 1 , Zimu Li 1 , Qili Huang 1 , Chendi Ding 2 , Li Yang 1 , Wenyan Wang 1 , Zhaoqing Shi 2 , Yao Yang 1 , Hongzhong Chen 1 , Lin Mei 2, 3 , Xiaowei Zeng 1
Advanced Functional Materials ( IF 18.5 ) Pub Date : 2023-09-15 , DOI: 10.1002/adfm.202307241 Wenfeng Zeng 1 , Zimu Li 1 , Qili Huang 1 , Chendi Ding 2 , Li Yang 1 , Wenyan Wang 1 , Zhaoqing Shi 2 , Yao Yang 1 , Hongzhong Chen 1 , Lin Mei 2, 3 , Xiaowei Zeng 1
Affiliation
|
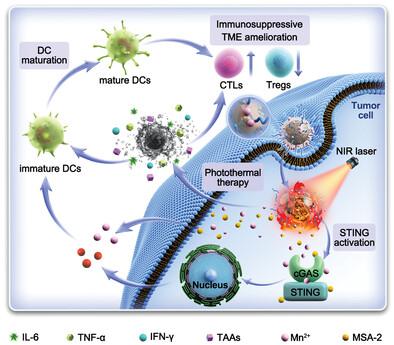
STING激动剂在各种恶性肿瘤中的治疗应用受到无法全身给药和免疫抑制肿瘤微环境等因素的限制。在此,这项工作报告了一种基于介孔聚多巴胺的多功能纳米平台,负载有STING激动剂MSA-2并与Mn 2+螯合,用于协同光热和基于STING激活的免疫治疗。该纳米平台有效地将 MSA-2 递送至肿瘤部位,并在光热效应的促进下通过酸降解智能地释放其内容物。此外,肿瘤组织的热消融可以诱导免疫原性细胞死亡,这有助于缓解免疫抑制的肿瘤微环境,从而增强MSA-2的疗效。此外,Mn 2+作为双重作用的 STING 敏化剂和 MRI 造影剂,不仅可以增强免疫反应,还可以对纳米平台进行实时 MRI 跟踪。事实证明,该策略在阻止原发性/转移性肿瘤和引发强大的肿瘤特异性免疫反应方面都非常有效。总的来说,本文重点介绍了一种有效的多功能纳米平台,用于全身递送 STING 激动剂,协同光热疗法和 STING 通路激活介导的免疫疗法,为优化癌症治疗的联合疗法提供新的思路和策略。

"点击查看英文标题和摘要"
更新日期:2023-09-15

"点击查看英文标题和摘要"




















































 京公网安备 11010802027423号
京公网安备 11010802027423号