当前位置:
X-MOL 学术
›
ACS Chem. Biol.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
他克林第一阶段生物转化和相关肝毒性:避免醌甲基化物形成的可能方法
ACS Chemical Biology ( IF 3.5 ) Pub Date : 2023-08-25 , DOI: 10.1021/acschembio.3c00219 Martin Novak 1, 2 , Marie Vajrychova 2 , Stefania Koutsilieri 3 , Despoina-Christina Sismanoglou 3 , Tereza Kobrlova 2 , Lukas Prchal 2 , Barbora Svobodova 2 , Jan Korabecny 2 , Tomas Zarybnicky 4 , Lucie Raisova-Stuchlikova 4 , Lenka Skalova 4 , Volker M Lauschke 3, 5, 6 , Radim Kučera 1 , Ondrej Soukup 2
ACS Chemical Biology ( IF 3.5 ) Pub Date : 2023-08-25 , DOI: 10.1021/acschembio.3c00219 Martin Novak 1, 2 , Marie Vajrychova 2 , Stefania Koutsilieri 3 , Despoina-Christina Sismanoglou 3 , Tereza Kobrlova 2 , Lukas Prchal 2 , Barbora Svobodova 2 , Jan Korabecny 2 , Tomas Zarybnicky 4 , Lucie Raisova-Stuchlikova 4 , Lenka Skalova 4 , Volker M Lauschke 3, 5, 6 , Radim Kučera 1 , Ondrej Soukup 2
Affiliation
|
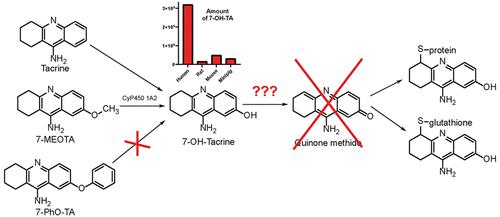
他克林作为抗阿尔茨海默病药物于2013年退出临床使用,主要原因是药物引起的肝损伤。他克林相关肝毒性的罪魁祸首被认为是 7-OH-他克林代谢物,它可能是醌甲基化物 (Q meth ) 的前体,可与细胞内 -SH 蛋白结合。在我们的研究中,使用了几种不同的动物和人类模型(肝微粒体、原代肝细胞和肝切片)来研究他克林及其7-取代类似物(7-甲氧基-、7-苯氧基-和7-苯氧基-)的生物转化和肝毒性。 -OH-他克林)。我们的目标是找到最合适的体外模型来研究他克林的肝毒性,并通过合理的结构修饰,开发出不易形成 Q meth的他克林衍生物。我们的结果表明,没有一个测试的动物模型能够准确模拟人类他克林的生物转化;然而,小鼠模型似乎比大鼠模型更合适。总体而言,在原代人肝细胞 (PHH) 的三维 (3D) 球体培养物中,他克林代谢的模拟最为准确。在该系统中,他克林和7-甲氧基他克林被羟基化为7-OH-他克林,而如预期的那样,仅形成痕量的7-苯氧基他克林。然而,令人惊讶的是,我们的研究表明,即使在调整剂量以达到相同的细胞内浓度后,7-OH-他克林的肝毒性也最小(7-OH-他克林<他克林<7-甲氧基他克林<7-苯氧基他克林)。所有研究的他克林衍生物都证实了人肝微粒体孵育后Q甲基半胱氨酸和 Q甲基谷胱甘肽加合物的形成,但这些发现在与 3D PHH 球体孵育后并未得到证实。因此,所提供的数据对先前假设的毒性机制提出了质疑,并且结果为化学修饰以提高新型他克林衍生物的安全性开辟了新途径。

"点击查看英文标题和摘要"
更新日期:2023-08-25

"点击查看英文标题和摘要"































 京公网安备 11010802027423号
京公网安备 11010802027423号