当前位置:
X-MOL 学术
›
Acta Pharm. Sin. B
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
通过在炎症反应中整合 IRF3 和 NF-κB,对血管内皮功能障碍进行非经典 STING-PERK 通路依赖性表观遗传调控
Acta Pharmaceutica Sinica B ( IF 14.7 ) Pub Date : 2023-08-17 , DOI: 10.1016/j.apsb.2023.08.015 Xuesong Li 1 , Xiang Chen 1 , Longbin Zheng 1, 2 , Minghong Chen 1 , Yunjia Zhang 1 , Ruigong Zhu 1 , Jiajing Chen 3 , Jiaming Gu 1 , Quanwen Yin 1 , Hong Jiang 1 , Xuan Wu 1 , Xian Ji 1 , Xin Tang 1 , Mengdie Dong 1 , Qingguo Li 4 , Yuanqing Gao 1 , Hongshan Chen 1, 4, 5, 6
Affiliation
|
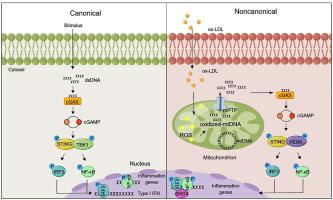
炎症驱动的内皮功能障碍是动脉粥样硬化的主要引发因素,但其潜在机制仍不清楚。在这里,我们报告干扰素基因的非经典刺激物(STING)-PKR 样 ER 激酶(PERK)通路在人类和小鼠动脉粥样硬化动脉中显着激活。通常,STING 激活会导致干扰素调节因子 3 (IRF3) 和核因子 kappa B (NF- κ B)/p65 的激活,从而促进IFN信号和炎症。相比之下,我们的研究表明,激活的非经典 STING-PERK 通路会增加支架蛋白溴结构域蛋白 4 (BRD4) 的表达,从而促进促炎细胞因子的近端启动子区域形成超级增强子,从而使这些细胞因子的反式激活成为可能。通过缩合过程整合激活的 IRF3 和 NF- κ B 来抑制细胞因子。内皮特异性 STING 和 BRD4 缺陷显着减少了斑块面积和炎症。从机制上讲,该途径是由线粒体 DNA (mtDNA)通过线粒体通透性转换孔 (mPTP) 泄漏而触发的,mPTP 是由电压依赖性阴离子通道 1 (VDAC1) 寡聚物在胆固醇氧化刺激下与氧化 mtDNA 相互作用形成的。特别是,与巨噬细胞相比,内皮 STING 激活在动脉粥样硬化中发挥着更显着的作用。我们提出了一种非经典的动脉粥样硬化 STING-PERK 通路依赖性表观遗传范例,它将 IRF3、NF- κ B 和 BRD4 整合到炎症反应中,为血管内皮功能障碍提供了新兴的治疗方式。

"点击查看英文标题和摘要"































 京公网安备 11010802027423号
京公网安备 11010802027423号