当前位置:
X-MOL 学术
›
J. Med. Chem.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
吲唑作为苯酚生物等排体:GluN2B 选择性 NMDA 受体拮抗剂的结构-亲和关系
Journal of Medicinal Chemistry ( IF 6.8 ) Pub Date : 2023-08-14 , DOI: 10.1021/acs.jmedchem.3c01161
Judith Lüken 1 , Gunnar Goerges 2 , Nadine Ritter 2, 3 , Paul Disse 2, 3 , Julian A Schreiber 1, 2 , Judith Schmidt 1 , Bastian Frehland 1 , Dirk Schepmann 1 , Guiscard Seebohm 2, 3 , Bernhard Wünsch 1, 3
Journal of Medicinal Chemistry ( IF 6.8 ) Pub Date : 2023-08-14 , DOI: 10.1021/acs.jmedchem.3c01161
Judith Lüken 1 , Gunnar Goerges 2 , Nadine Ritter 2, 3 , Paul Disse 2, 3 , Julian A Schreiber 1, 2 , Judith Schmidt 1 , Bastian Frehland 1 , Dirk Schepmann 1 , Guiscard Seebohm 2, 3 , Bernhard Wünsch 1, 3
Affiliation
|
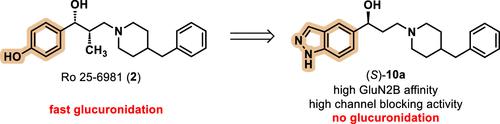
含有 GluN2B 亚基的 NMDA 受体的负变构调节可防止过度刺激,从而产生神经保护作用。由于显着的负变构调节剂的苯酚易于快速葡萄糖醛酸化,因此设想用吲唑替代其生物等排。合成的关键步骤是未保护的碘吲唑与炔丙基哌啶衍生物的 Sonogashira 反应。炔基部分的修饰允许引入几个官能团。合成的吲唑显示出非常高的 GluN2B 亲和力,但对 σ 受体的选择性有限。分子动力学模拟揭示了与类似酚类相同的与艾芬地尔结合位点的分子相互作用。在双电极电压钳实验中,对映体 3-(4-benzylpiperidin-1-yl)-1-(1 H -indazol-5-yl)propan-1-ols ( S )- 10a和 ( R )- 10a表现出比艾芬地尔更高的抑制活性。与酚类 GluN2B 拮抗剂相反,吲唑不与葡萄糖醛酸缀合。可以得出结论,有效的GluN2B拮抗剂的苯酚可以通过生物电子等排被吲唑取代,保留高GluN2B亲和力和活性,但抑制葡萄糖醛酸化。

"点击查看英文标题和摘要"
更新日期:2023-08-14

"点击查看英文标题和摘要"

































 京公网安备 11010802027423号
京公网安备 11010802027423号