当前位置:
X-MOL 学术
›
Mol. Ther. Methods Clin. Dev.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
建立 UGT1A1 敲除人 iPS 衍生的肝类器官,用于 UGT1A1 特异性动力学和毒性评估
Molecular Therapy - Methods & Clinical Development ( IF 4.6 ) Pub Date : 2023-08-11 , DOI: 10.1016/j.omtm.2023.08.003 Tomohiro Shintani 1 , Chiharu Imamura 2 , Yukiko Ueyama-Toba 1, 2, 3, 4 , Jumpei Inui 1 , Akira Watanabe 2 , Hiroyuki Mizuguchi 1, 2, 3, 4, 5, 6
Molecular Therapy - Methods & Clinical Development ( IF 4.6 ) Pub Date : 2023-08-11 , DOI: 10.1016/j.omtm.2023.08.003 Tomohiro Shintani 1 , Chiharu Imamura 2 , Yukiko Ueyama-Toba 1, 2, 3, 4 , Jumpei Inui 1 , Akira Watanabe 2 , Hiroyuki Mizuguchi 1, 2, 3, 4, 5, 6
Affiliation
|
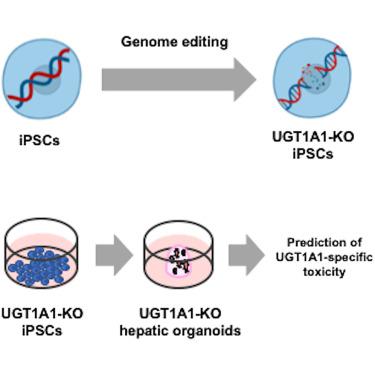
尿苷二磷酸葡萄糖醛酸基转移酶(UGT)在肝脏中高表达,参与许多药物的代谢。特别是,UGT1A1 具有基因多态性,会导致活性降低,从而导致药物引起的肝毒性。因此,需要一种能够准确预测涉及UGT1A1的药物动力学的评估系统。然而,由于缺乏UGT1A1选择性抑制剂,因此不存在这样的评估系统。在这里,利用人类诱导多能干(iPS)细胞、基因组编辑技术和类器官技术,我们生成了 UGT1A1 敲除的人 iPS 肝细胞来源的肝脏类器官(UGT1A1-KO i-HO)作为 UGT1A1 特异性动力学和毒性的模型评估。 i-HOs 显示出比人 iPS 细胞来源的肝细胞样细胞 (iPS-HLC) 更高的包括 UGT1A1 在内的许多药物代谢酶的基因表达,表明肝类器官技术可改善肝功能。野生型 (WT) i-HO 显示出与原代人(冷冻保存)肝细胞相似的 UGT1A1 活性水平,而 UGT1A1-KO i-HO 完全丧失了活性。此外,为了评估该模型是否可用于预测药物引起的肝毒性,将 UGT1A1-KO i-HO 暴露于抗癌药物伊立替康的活性代谢物 SN-38 和对乙酰氨基酚,并证实这些细胞可以预测 UGT1A1 -介导的毒性。因此,我们成功地生成了能够评估 UGT1A1 特异性动力学和毒性的模型细胞。

"点击查看英文标题和摘要"
更新日期:2023-08-11

"点击查看英文标题和摘要"































 京公网安备 11010802027423号
京公网安备 11010802027423号