Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
脂肪 METTL14 诱导的 N6-甲基腺苷通过抑制肾上腺素能信号传导和脂肪分解促进肥胖、胰岛素抵抗和 NAFLD β
Advanced Science ( IF 14.3 ) Pub Date : 2023-08-01 , DOI: 10.1002/advs.202301645 Qianqian Kang 1, 2 , Xiaorong Zhu 1, 3 , Decheng Ren 4 , Alexander Ky 5 , Ormond A MacDougald 1, 2, 6 , Robert W O'Rourke 5, 7 , Liangyou Rui 1, 2, 6
Affiliation
|
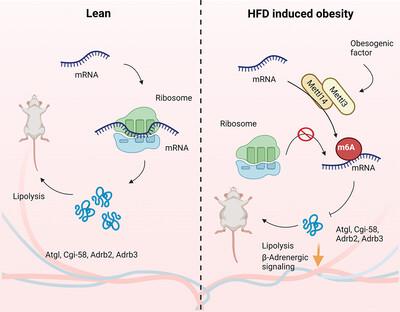
白色脂肪组织 (WAT) 脂肪分解释放游离脂肪酸作为关键能量物质,以支持禁食、寒冷暴露和运动中的新陈代谢。Atgl 与 Cgi-58 协同催化第一个脂解反应。交感神经系统 (SNS) 通过神经递质去甲肾上腺素刺激脂肪分解,去甲肾上腺素激活脂肪细胞β肾上腺素能受体 (Adrb1-3)。在肥胖中,脂肪 Adrb 信号传导和脂肪分解受损,导致致病性 WAT 扩增;然而,人们对底层机制仍然知之甚少。最近的研究强调了基于 N6-甲基腺苷 (m6A) 的 RNA 修饰在健康和疾病中的重要性。METTL14 与 METTL3 异二聚化,形成 RNA 甲基转移酶复合物,将 m6A 安装在转录本中。在这里,这项工作表明脂肪 Mettl3 和 Mettl14 受禁食、再喂养和胰岛素的影响,并在高脂饮食 (HFD) 诱导的肥胖中上调。肥胖时脂肪 Adrb2 、 Adrb3 、 Atgl 和 Cgi-58 转录本 m6A 含量升高。Mettl14 消融降低这些转录本的 m6A 含量并增加它们在脂肪细胞中的翻译和蛋白质水平,从而增加 Adrb 信号传导和脂肪分解。具有脂肪细胞特异性 Mettl14 缺失的小鼠对 HFD 诱导的肥胖、胰岛素抵抗、葡萄糖耐受不良和非酒精性脂肪肝 (NAFLD) 具有抵抗力。这些结果揭示了控制 Adrb 信号传导和脂肪分解的 METTL14/m6A/翻译通路。基于 METTL14/m6A 的表观转录组学重编程损害脂肪 Adrb 信号传导和脂肪分解,促进肥胖、NAFLD 和代谢疾病。

"点击查看英文标题和摘要"















































 京公网安备 11010802027423号
京公网安备 11010802027423号