Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
H因子对补体C3的细胞自主调节限制巨噬细胞胞吞作用并加剧动脉粥样硬化
Immunity ( IF 25.5 ) Pub Date : 2023-07-26 , DOI: 10.1016/j.immuni.2023.06.026 Máté G Kiss 1 , Nikolina Papac-Miličević 2 , Florentina Porsch 1 , Dimitrios Tsiantoulas 3 , Tim Hendrikx 2 , Minoru Takaoka 4 , Huy Q Dinh 5 , Marie-Sophie Narzt 6 , Laura Göderle 2 , Mária Ozsvár-Kozma 2 , Michael Schuster 7 , Nikolaus Fortelny 8 , Anastasiya Hladik 9 , Sylvia Knapp 9 , Florian Gruber 6 , Matthew C Pickering 10 , Christoph Bock 11 , Filip K Swirski 12 , Klaus Ley 13 , Alma Zernecke 14 , Clément Cochain 15 , Claudia Kemper 16 , Ziad Mallat 17 , Christoph J Binder 1
Affiliation
|
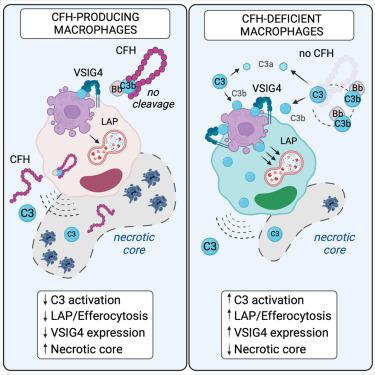
补体因子 H (CFH) 负向调节补体成分 3 (C3) 的消耗,从而限制补体激活。 CFH的基因变异易患慢性炎症性疾病。在这里,我们研究了 CFH 对动脉粥样硬化发展的影响。在动脉粥样硬化小鼠模型中,CFH 缺乏以 C3 依赖性方式限制斑块坏死。单核细胞来源的炎症巨噬细胞中 CFH 的缺失会传播不受控制的细胞自主 C3 消耗,而没有下游 C5 激活和增强的胞吞能力。在白细胞中, Cfh表达仅限于单核细胞和巨噬细胞,在炎症过程中表达增加,并且与细胞内 C3 的积累一致。巨噬细胞衍生的 CFH 足以抑制炎症的消退,而动脉粥样硬化易发小鼠中 CFH 的造血缺失促进了病变的胞吞作用并减小了斑块大小。此外,我们在人动脉粥样硬化斑块中发现了表达 C3 和 CFH 的单核细胞来源的炎症巨噬细胞。我们的研究结果揭示了CFH以细胞自主方式控制巨噬细胞胞内C3水平的调节轴,证明了现场补体调节在炎症性疾病发病机制中的重要性。

"点击查看英文标题和摘要"































 京公网安备 11010802027423号
京公网安备 11010802027423号