当前位置:
X-MOL 学术
›
J. Am. Chem. Soc.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Oxidation and Phenolysis of Peptide/Protein C-Terminal Hydrazides Afford Salicylaldehyde Ester Surrogates for Chemical Protein Synthesis
Journal of the American Chemical Society ( IF 14.4 ) Pub Date : 2023-07-20 , DOI: 10.1021/jacs.3c05190 Shaomin Lin 1 , Zeyuan Mo 1 , Peng Wang 1 , Chunmao He 1
Journal of the American Chemical Society ( IF 14.4 ) Pub Date : 2023-07-20 , DOI: 10.1021/jacs.3c05190 Shaomin Lin 1 , Zeyuan Mo 1 , Peng Wang 1 , Chunmao He 1
Affiliation
|
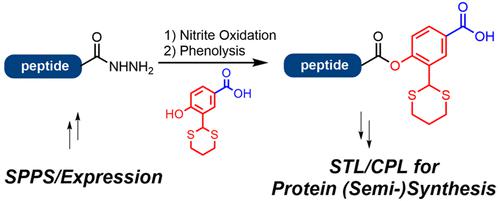
With the growing popularity of serine/threonine ligation (STL) and cysteine/penicillamine ligation (CPL) in chemical protein synthesis, facile and general approaches for the preparation of peptide salicylaldehyde (SAL) esters are urgently needed, especially those viable for obtaining expressed protein SAL esters. Herein, we report the access of SAL ester surrogates from peptide hydrazides (obtained either synthetically or recombinantly) via nitrite oxidation and phenolysis by 3-(1,3-dithian-2-yl)-4-hydroxybenzoic acid (SAL(−COOH)PDT). The resulting peptide SAL(−COOH)PDT esters can be activated to afford the reactive peptide SAL(−COOH) esters for subsequent STL/CPL. While being operationally simple for both synthetic peptides and expressed proteins, the current strategy facilitates convergent protein synthesis and combined application of STL with NCL. The generality of the strategy is showcased by the N-terminal ubiquitination of the growth arrest and DNA damage-inducible protein (Gadd45a), the efficient synthesis of ubiquitin-like protein 5 (UBL-5) via a combined N-to-C NCL-STL strategy, and the C-to-N semisynthesis of a myoglobin (Mb) variant.
中文翻译:

肽/蛋白质 C 端酰肼的氧化和酚解为化学蛋白质合成提供水杨醛酯替代物
随着丝氨酸/苏氨酸连接(STL)和半胱氨酸/青霉胺连接(CPL)在化学蛋白质合成中的日益普及,迫切需要用于制备肽水杨醛(SAL)酯的简便且通用的方法,特别是那些可行的获得表达蛋白质的方法SAL 酯。在此,我们报告了通过亚硝酸盐氧化和 3-(1,3-二噻安-2-基)-4-羟基苯甲酸 (SAL(−COOH)) 的酚解从肽酰肼(合成或重组获得)中获得 SAL 酯替代物太平洋夏令时)。生成的肽 SAL(-COOH) PDT酯可以被激活,为后续的 STL/CPL 提供反应性肽 SAL(-COOH) 酯。虽然合成肽和表达蛋白的操作都很简单,但当前的策略有利于蛋白质合成的收敛以及 STL 与 NCL 的组合应用。该策略的通用性通过生长停滞和 DNA 损伤诱导蛋白 (Gadd45a) 的 N 端泛素化、通过组合 N-to-C NCL 有效合成泛素样蛋白 5 (UBL-5) 来展示。 -STL 策略,以及肌红蛋白 (Mb) 变体的 C-N 半合成。
更新日期:2023-07-20
中文翻译:

肽/蛋白质 C 端酰肼的氧化和酚解为化学蛋白质合成提供水杨醛酯替代物
随着丝氨酸/苏氨酸连接(STL)和半胱氨酸/青霉胺连接(CPL)在化学蛋白质合成中的日益普及,迫切需要用于制备肽水杨醛(SAL)酯的简便且通用的方法,特别是那些可行的获得表达蛋白质的方法SAL 酯。在此,我们报告了通过亚硝酸盐氧化和 3-(1,3-二噻安-2-基)-4-羟基苯甲酸 (SAL(−COOH)) 的酚解从肽酰肼(合成或重组获得)中获得 SAL 酯替代物太平洋夏令时)。生成的肽 SAL(-COOH) PDT酯可以被激活,为后续的 STL/CPL 提供反应性肽 SAL(-COOH) 酯。虽然合成肽和表达蛋白的操作都很简单,但当前的策略有利于蛋白质合成的收敛以及 STL 与 NCL 的组合应用。该策略的通用性通过生长停滞和 DNA 损伤诱导蛋白 (Gadd45a) 的 N 端泛素化、通过组合 N-to-C NCL 有效合成泛素样蛋白 5 (UBL-5) 来展示。 -STL 策略,以及肌红蛋白 (Mb) 变体的 C-N 半合成。




















































 京公网安备 11010802027423号
京公网安备 11010802027423号