Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
铁死亡和坏死性凋亡产生自体肿瘤细胞裂解物与联合免疫佐剂共同递送作为抗肿瘤免疫的个性化原位纳米疫苗
ACS Nano ( IF 15.8 ) Pub Date : 2023-07-19 , DOI: 10.1021/acsnano.3c00901 Wanrui Shi 1 , Wenjie Feng 1 , Siyuan Li 1 , Yanqi Cui 1 , Shuwei Liu 2 , Huan Jiang 3 , Yi Liu 1 , Hao Zhang 1, 2, 4
ACS Nano ( IF 15.8 ) Pub Date : 2023-07-19 , DOI: 10.1021/acsnano.3c00901 Wanrui Shi 1 , Wenjie Feng 1 , Siyuan Li 1 , Yanqi Cui 1 , Shuwei Liu 2 , Huan Jiang 3 , Yi Liu 1 , Hao Zhang 1, 2, 4
Affiliation
|
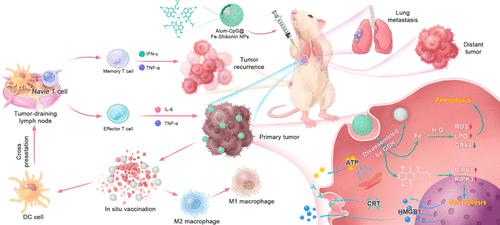
基于纳米疫苗的免疫治疗被认为是刺激宿主免疫系统识别和消灭肿瘤细胞以及建立长期免疫记忆以防止肿瘤复发和转移的主要支柱。然而,抗原的弱特异性和低交叉呈递以及肿瘤组织的免疫抑制微环境仍然是肿瘤纳米疫苗充分发挥治疗性能的主要障碍。在此,我们设计并构建了负载胞嘧啶鸟嘌呤二核苷酸(CpG)寡脱氧核苷酸(ODN)的羟基磷酸铝纳米颗粒,该纳米颗粒被铁紫草素金属酚网络(MPN)覆盖(Alum-CpG@Fe-紫草素纳米粒子)作为个性化原位抗肿瘤纳米疫苗免疫。被肿瘤细胞内化后,Fe-Shikonin MPNs 的外壳将分解为 Fe 2+和 Shikonin,通过铁死亡和坏死性凋亡引发肿瘤细胞的免疫原性细胞死亡。然后,垂死的肿瘤细胞释放的自体肿瘤细胞裂解物将被Alum NPs吸收,并与CpG ODN在时间和空间上共同递送至专业抗原呈递细胞,以激活多步级联抗肿瘤免疫反应,包括树突状细胞成熟、抗原交叉呈递、自然杀伤细胞和细胞毒性 T 淋巴细胞浸润,以及肿瘤相关巨噬细胞复极化。受益于 Alum NPs、CpG ODN 和 Fe-Shikonin MPNs 的协同作用,我们的 Alum-CpG@Fe-Shikonin NPs 在根除原发肿瘤方面表现出强烈的细胞毒性和精确的选择性,对抑制远处肿瘤具有强烈的远隔作用,并且具有长效作用。长期免疫记忆作用可预防肿瘤转移和复发。由于我们的报告提供了一种原位充分利用自体肿瘤细胞裂解物的可行策略,该裂解物呈现患者个人表位的全谱,而无需复杂的离体过程,例如提取、纯化和测序,因此它可能会促进肿瘤细胞裂解物的发展。用于抗肿瘤免疫的个性化纳米疫苗。

"点击查看英文标题和摘要"
更新日期:2023-07-19

"点击查看英文标题和摘要"































 京公网安备 11010802027423号
京公网安备 11010802027423号