当前位置:
X-MOL 学术
›
ACS Biomater. Sci. Eng.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
pH 响应、逐层电荷反转纳米颗粒表面增强生物膜渗透和根除
ACS Biomaterials Science & Engineering ( IF 5.4 ) Pub Date : 2023-06-30 , DOI: 10.1021/acsbiomaterials.3c00481 Elad Deiss-Yehiely 1, 2 , Gerardo Cárcamo-Oyarce 3 , Adam G Berger 2, 4, 5 , Katharina Ribbeck 3 , Paula T Hammond 2, 4, 6
Affiliation
|
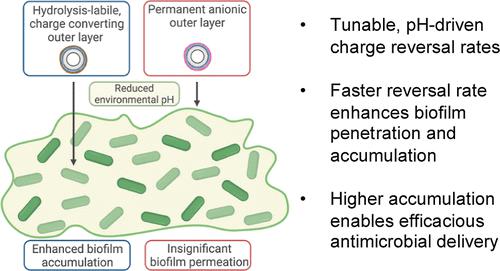
根深蒂固在生物膜内的微生物可以承受高浓度 1000 倍的抗生素,部分原因是粘性细胞外基质会隔离和减弱抗菌活性。与单独的游离药物相比,基于纳米颗粒 (NP) 的疗法可以帮助在整个生物膜中提供更高的局部浓度,从而提高疗效。规范的设计标准规定带正电荷的纳米颗粒可以多价结合阴离子生物膜成分并增加生物膜渗透。然而,阳离子颗粒是有毒的,并且会迅速从体内循环中清除,限制了它们的使用。因此,我们试图设计 pH 响应型纳米颗粒,将其表面电荷从负变为正,以响应生物膜 pH 微环境的降低。我们合成了一系列 pH 依赖性、可水解聚合物,并采用逐层 (LbL) 静电组装方法来制造以这些聚合物作为最外表面的生物相容性纳米粒子。 NP 电荷转化率由聚合物亲水性和侧链结构决定,在实验时间内从数小时到无法检测到。 LbL NP 具有越来越快的电荷转换率,更有效地渗透并在野生型 (PAO1) 和突变体过表达生物量 (Δ wspF )铜绿假单胞菌生物膜中积累。最后,妥布霉素(一种已知被阴离子生物膜成分捕获的抗生素)被加载到 LbL NP 的最后一层。与最慢的电荷转换器和游离妥布霉素相比,最快的电荷转换 NP 的 Δ wspF集落形成单位减少了 3.2 倍。 这些研究为设计可响应基质相互作用的生物膜穿透纳米颗粒提供了一个框架,最终提高了抗菌药物的有效输送。

"点击查看英文标题和摘要"

































 京公网安备 11010802027423号
京公网安备 11010802027423号