当前位置:
X-MOL 学术
›
J. Org. Chem.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Synthesis and Evaluation of Diguanosine Cap Analogs Modified at the C8-Position by Suzuki–Miyaura Cross-Coupling: Discovery of 7-Methylguanosine-Based Molecular Rotors
The Journal of Organic Chemistry ( IF 3.3 ) Pub Date : 2023-05-20 , DOI: 10.1021/acs.joc.3c00126 Blazej A Wojtczak 1 , Marcelina Bednarczyk 1, 2 , Pawel J Sikorski 1 , Anna Wojtczak 2 , Piotr Surynt 1, 2 , Joanna Kowalska 2 , Jacek Jemielity 1
The Journal of Organic Chemistry ( IF 3.3 ) Pub Date : 2023-05-20 , DOI: 10.1021/acs.joc.3c00126 Blazej A Wojtczak 1 , Marcelina Bednarczyk 1, 2 , Pawel J Sikorski 1 , Anna Wojtczak 2 , Piotr Surynt 1, 2 , Joanna Kowalska 2 , Jacek Jemielity 1
Affiliation
|
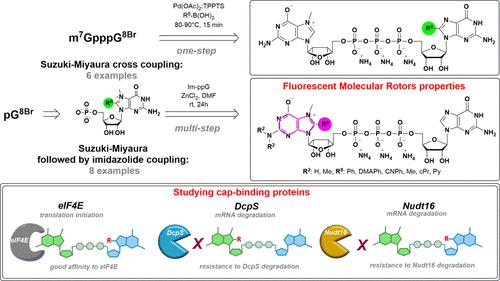
Chemical modifications of the mRNA cap structure can enhance the stability, translational properties, and half-life of mRNAs, thereby altering the therapeutic properties of synthetic mRNA. However, cap structure modification is challenging because of the instability of the 5′-5′-triphosphate bridge and N7-methylguanosine. The Suzuki–Miyaura cross-coupling reaction between boronic acid and halogen compound is a mild, convenient, and potentially applicable approach for modifying biomolecules. Herein, we describe two methods to synthesize C8-modified cap structures using the Suzuki–Miyaura cross-coupling reaction. Both methods employed phosphorimidazolide chemistry to form the 5′,5′-triphosphate bridge. However, in the first method, the introduction of the modification via the Suzuki–Miyaura cross-coupling reaction at the C8 position occurs postsynthetically, at the dinucleotide level, whereas in the second method, the modification was introduced at the level of the nucleoside 5′-monophosphate, and later, the triphosphate bridge was formed. Both methods were successfully applied to incorporate six different groups (methyl, cyclopropyl, phenyl, 4-dimethylaminophenyl, 4-cyanophenyl, and 1-pyrene) into either the m7G or G moieties of the cap structure. Aromatic substituents at the C8-position of guanosine form a push–pull system that exhibits environment-sensitive fluorescence. We demonstrated that this phenomenon can be harnessed to study the interaction with cap-binding proteins, e.g., eIF4E, DcpS, Nudt16, and snurportin.
中文翻译:

通过 Suzuki-Miyaura 交叉偶联在 C8 位修饰的二鸟苷帽类似物的合成和评价:基于 7-甲基鸟苷的分子转子的发现
mRNA帽结构的化学修饰可以增强mRNA的稳定性、翻译特性和半衰期,从而改变合成mRNA的治疗特性。然而,由于 5'-5'-三磷酸桥和 N7-甲基鸟苷的不稳定,帽结构修饰具有挑战性。硼酸和卤素化合物之间的铃木-宫浦交叉偶联反应是一种温和、方便且具有潜在适用性的生物分子修饰方法。在此,我们描述了两种使用铃木-宫浦交叉偶联反应合成 C8 修饰帽结构的方法。两种方法均采用磷咪唑化学来形成 5',5'-三磷酸桥。然而,在第一种方法中,通过引入修改C8位置的Suzuki-Miyaura交叉偶联反应发生在合成后的二核苷酸水平上,而在第二种方法中,修饰是在核苷5'-单磷酸水平上引入的,随后形成了三磷酸桥。两种方法都成功地将六个不同的基团(甲基、环丙基、苯基、4-二甲基氨基苯基、4-氰基苯基和1-芘)并入帽结构的 m 7 G 或 G部分。鸟苷 C8 位的芳香族取代基形成推拉系统,表现出环境敏感的荧光。我们证明,可以利用这种现象来研究与帽结合蛋白(例如,eIF4E、DcpS、Nudt16 和 snurportin )的相互作用。
更新日期:2023-05-20
中文翻译:

通过 Suzuki-Miyaura 交叉偶联在 C8 位修饰的二鸟苷帽类似物的合成和评价:基于 7-甲基鸟苷的分子转子的发现
mRNA帽结构的化学修饰可以增强mRNA的稳定性、翻译特性和半衰期,从而改变合成mRNA的治疗特性。然而,由于 5'-5'-三磷酸桥和 N7-甲基鸟苷的不稳定,帽结构修饰具有挑战性。硼酸和卤素化合物之间的铃木-宫浦交叉偶联反应是一种温和、方便且具有潜在适用性的生物分子修饰方法。在此,我们描述了两种使用铃木-宫浦交叉偶联反应合成 C8 修饰帽结构的方法。两种方法均采用磷咪唑化学来形成 5',5'-三磷酸桥。然而,在第一种方法中,通过引入修改C8位置的Suzuki-Miyaura交叉偶联反应发生在合成后的二核苷酸水平上,而在第二种方法中,修饰是在核苷5'-单磷酸水平上引入的,随后形成了三磷酸桥。两种方法都成功地将六个不同的基团(甲基、环丙基、苯基、4-二甲基氨基苯基、4-氰基苯基和1-芘)并入帽结构的 m 7 G 或 G部分。鸟苷 C8 位的芳香族取代基形成推拉系统,表现出环境敏感的荧光。我们证明,可以利用这种现象来研究与帽结合蛋白(例如,eIF4E、DcpS、Nudt16 和 snurportin )的相互作用。

































 京公网安备 11010802027423号
京公网安备 11010802027423号