当前位置:
X-MOL 学术
›
ACS Biomater. Sci. Eng.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
STING/TBK1 调节巨噬细胞炎症和钛颗粒诱导的骨溶解
ACS Biomaterials Science & Engineering ( IF 5.4 ) Pub Date : 2023-05-03 , DOI: 10.1021/acsbiomaterials.2c01509 Zhuji Ouyang 1 , Jing Xu 1 , Taihe Liu 1 , Sipeng Lin 1 , Yujun Sun 1 , Yuhsi Huang 1 , Zhongcan Zheng 1 , Gang Zeng 1 , Changchuan Li 1 , Shixun Li 1 , Yue Ding 1
ACS Biomaterials Science & Engineering ( IF 5.4 ) Pub Date : 2023-05-03 , DOI: 10.1021/acsbiomaterials.2c01509 Zhuji Ouyang 1 , Jing Xu 1 , Taihe Liu 1 , Sipeng Lin 1 , Yujun Sun 1 , Yuhsi Huang 1 , Zhongcan Zheng 1 , Gang Zeng 1 , Changchuan Li 1 , Shixun Li 1 , Yue Ding 1
Affiliation
|
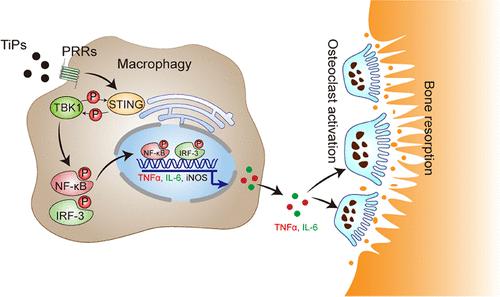
由假体衍生的磨损颗粒引起的巨噬细胞炎症反应是人工关节失效的主要原因。然而,磨损颗粒引发巨噬细胞炎症的机制尚未完全阐明。先前的研究已经确定 TANK 结合激酶 1 (TBK1) 和干扰素基因刺激物 (STING) 是炎症和自身免疫性疾病的潜在因素。在这里,我们发现无菌性松动 (AL) 患者的滑膜中 TBK1 和 STING 均增加,并在钛颗粒 (TiPs) 刺激的巨噬细胞中被激活。慢病毒介导的 TBK 或 STING 敲低显着抑制了巨噬细胞的炎症作用,而 TBK 或 STING 的过表达产生相反的结果。具体来说,STING/TBK1 促进 NF-κB 和 IRF3 通路的激活以及巨噬细胞 M1 极化。为了进一步验证,我们构建了一个小鼠颅骨骨溶解模型用于体内试验,我们发现注射 STING 过表达的慢病毒会加剧骨溶解和炎症,而这会被 TBK1 敲低注射所抵消。总之,STING/TBK1 通过协调 NF-κB 和 IRF3 通路的激活以及 M1 极化来增强 TiP 诱导的巨噬细胞炎症和骨质溶解,这表明 STING/TBK1 是预防假体 AL 的潜在治疗靶点。

"点击查看英文标题和摘要"
更新日期:2023-05-03

"点击查看英文标题和摘要"































 京公网安备 11010802027423号
京公网安备 11010802027423号