Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
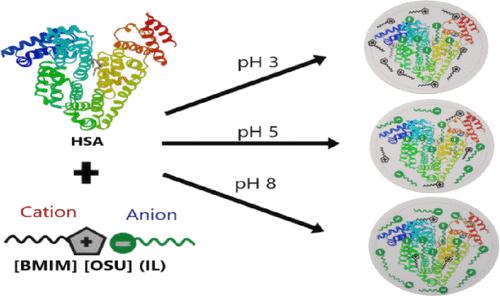
pH-Induced Biophysical Perspectives of Binding of Surface-Active Ionic Liquid [BMIM][OSU] with HSA and Dynamics of the Formed Complex
Langmuir ( IF 3.7 ) Pub Date : 2023-03-01 , DOI: 10.1021/acs.langmuir.2c03472
R Ravikanth Reddy 1, 2 , Debasish Saha 3 , Animesh Pan 4 , Vinod Kumar Aswal 3 , Soumya Sundar Mati 5 , Satya Priya Moulik 6 , Bandaru V N Phani Kumar 1, 2
Langmuir ( IF 3.7 ) Pub Date : 2023-03-01 , DOI: 10.1021/acs.langmuir.2c03472
R Ravikanth Reddy 1, 2 , Debasish Saha 3 , Animesh Pan 4 , Vinod Kumar Aswal 3 , Soumya Sundar Mati 5 , Satya Priya Moulik 6 , Bandaru V N Phani Kumar 1, 2
Affiliation
|
The influence of pH on the human serum albumin (HSA) interaction with ionic liquid (IL)1-butyl 3-methylimidazolium octyl sulfate ([BMIM][OSU]) at its sub-micellar concentration of 5 mM (well below CMC ∼31 mM at 25 °C) in aqueous solution has been monitored employing different methods, viz., circular dichroism (CD), fluorescence, electrokinetic determination of the zeta potential (ZP), nuclear magnetic resonance (NMR), small-angle neutron scattering (SANS), and molecular docking (MD). CD analysis indicated a noticeable reduction of the α-helical content of HSA by IL at pH 3. A significant interaction of the anionic part of IL with HSA was evident from the 1H chemical shifts and saturation transfer difference (STD) NMR. A strong binding between IL and HSA was observed at pH 3 relative to pH 5, revealing the importance of electrostatic and hydrophobic interactions assessed from global binding affinities and molecular correlation times derived from STD NMR and a combined selective/nonselective spin-relaxation analysis, respectively. ZP data supported the electrostatic interaction between HSA and the anionic part of IL. The nature of IL self-diffusion with HSA was assessed from the translational self-diffusion coefficients by pulse field gradient NMR. SANS results revealed the formation of prolate ellipsoidal geometry of the IL–HSA complex. MD identified the preferential binding sites of IL to the tryptophan centers on HSA. The association of IL with HSA was supported by fluorescence measurements, in addition to the structural changes that occurred in the protein by the interaction with IL. The anionic part of IL contributed a major interaction with HSA at the pH levels of study (3, 5, 8, and 11.4); at pH > 8 (effectively 11.4), the protein also interacted weakly with the cationic component of IL.
中文翻译:

pH 诱导的表面活性离子液体 [BMIM][OSU] 与 HSA 结合的生物物理学观点和形成的复合物的动力学
pH 值对人血清白蛋白 (HSA) 与离子液体 (IL)1-丁基 3-甲基咪唑鎓辛基硫酸盐 ([BMIM][OSU]) 相互作用的影响,其亚胶束浓度为 5 mM(远低于 CMC ~31 mM at 25 °C) 在水溶液中的监测采用不同的方法,即圆二色性 (CD)、荧光、zeta 电位 (ZP) 的电动测定、核磁共振 (NMR)、小角中子散射 ( SANS)和分子对接(MD)。CD 分析表明,在 pH 3 时,IL 显着降低了 HSA 的 α-螺旋含量。IL 的阴离子部分与 HSA 的显着相互作用从1H 化学位移和饱和转移差 (STD) NMR。在 pH 3 相对于 pH 5 时观察到 IL 和 HSA 之间的强结合,揭示了静电和疏水相互作用的重要性,这些相互作用分别从 STD NMR 和组合的选择性/非选择性自旋弛豫分析得出的全局结合亲和力和分子相关时间进行评估. ZP 数据支持 HSA 和 IL 的阴离子部分之间的静电相互作用。通过脉冲场梯度 NMR 从平移自扩散系数评估 IL 自扩散与 HSA 的性质。SANS 结果揭示了 IL-HSA 复合物的长椭球几何形状的形成。MD 确定了 IL 与 HSA 上色氨酸中心的优先结合位点。荧光测量支持 IL 与 HSA 的关联,除了通过与 IL 的相互作用而在蛋白质中发生的结构变化。IL 的阴离子部分在研究的 pH 水平(3、5、8 和 11.4)下与 HSA 产生了主要相互作用;在 pH > 8(有效 11.4)时,蛋白质也与 IL 的阳离子成分相互作用较弱。
更新日期:2023-03-01
中文翻译:

pH 诱导的表面活性离子液体 [BMIM][OSU] 与 HSA 结合的生物物理学观点和形成的复合物的动力学
pH 值对人血清白蛋白 (HSA) 与离子液体 (IL)1-丁基 3-甲基咪唑鎓辛基硫酸盐 ([BMIM][OSU]) 相互作用的影响,其亚胶束浓度为 5 mM(远低于 CMC ~31 mM at 25 °C) 在水溶液中的监测采用不同的方法,即圆二色性 (CD)、荧光、zeta 电位 (ZP) 的电动测定、核磁共振 (NMR)、小角中子散射 ( SANS)和分子对接(MD)。CD 分析表明,在 pH 3 时,IL 显着降低了 HSA 的 α-螺旋含量。IL 的阴离子部分与 HSA 的显着相互作用从1H 化学位移和饱和转移差 (STD) NMR。在 pH 3 相对于 pH 5 时观察到 IL 和 HSA 之间的强结合,揭示了静电和疏水相互作用的重要性,这些相互作用分别从 STD NMR 和组合的选择性/非选择性自旋弛豫分析得出的全局结合亲和力和分子相关时间进行评估. ZP 数据支持 HSA 和 IL 的阴离子部分之间的静电相互作用。通过脉冲场梯度 NMR 从平移自扩散系数评估 IL 自扩散与 HSA 的性质。SANS 结果揭示了 IL-HSA 复合物的长椭球几何形状的形成。MD 确定了 IL 与 HSA 上色氨酸中心的优先结合位点。荧光测量支持 IL 与 HSA 的关联,除了通过与 IL 的相互作用而在蛋白质中发生的结构变化。IL 的阴离子部分在研究的 pH 水平(3、5、8 和 11.4)下与 HSA 产生了主要相互作用;在 pH > 8(有效 11.4)时,蛋白质也与 IL 的阳离子成分相互作用较弱。

































 京公网安备 11010802027423号
京公网安备 11010802027423号