当前位置:
X-MOL 学术
›
Mater. Today Bio
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
用于三阴性乳腺癌治疗的光动力介导的谷氨酰胺代谢干预纳米药物
Materials Today Bio ( IF 8.7 ) Pub Date : 2023-02-15 , DOI: 10.1016/j.mtbio.2023.100577 Cancan Yu 1 , Ningning Wang 1 , Xiangwu Chen 1 , Yue Jiang 1 , Yuxia Luan 1 , Wen Qin 2 , Wenxiu He 1

"点击查看英文标题和摘要"
更新日期:2023-02-18
Materials Today Bio ( IF 8.7 ) Pub Date : 2023-02-15 , DOI: 10.1016/j.mtbio.2023.100577 Cancan Yu 1 , Ningning Wang 1 , Xiangwu Chen 1 , Yue Jiang 1 , Yuxia Luan 1 , Wen Qin 2 , Wenxiu He 1
Affiliation
|
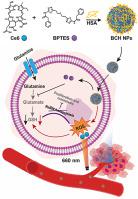
“谷氨酰胺成瘾”是三阴性乳腺癌(TNBC)的独特特征,对谷氨酰胺的需求更高,更容易出现谷氨酰胺耗竭。谷氨酰胺可被谷氨酰胺酶(GLS)水解为谷氨酸,合成谷胱甘肽(GSH),谷胱甘肽是加速TNBC增殖的谷氨酰胺代谢途径的重要下游。因此,谷氨酰胺代谢干预表明对 TNBC 具有潜在的治疗作用。然而,GLS 抑制剂的作用受到谷氨酰胺抗性及其自身的不稳定性和不溶性的阻碍。因此,协调谷氨酰胺代谢干预以扩大 TNBC 治疗具有重要意义。不幸的是,这样的纳米平台还没有实现。在此处,我们报道了一种自组装纳米平台 (BCH NPs),其核心是 GLS 抑制剂 Bis-2-(5-phenylacetamido-1,3,4-thiadiazol-2-yl) ethyl sulfide (BPTES) 和光敏剂 Chlorin e6 (Ce6 ) 和人血清白蛋白 (HSA) 的外壳,能够有效协调谷氨酰胺代谢干预以用于 TNBC 治疗。BPTES通过抑制GLS的活性来阻断谷氨酰胺代谢途径,从而抑制GSH的产生从而放大Ce6的光动力效应。而Ce6不仅通过产生过量的活性氧(ROS)直接杀死肿瘤细胞,而且还消耗GSH破坏氧化还原平衡,从而在发生谷氨酰胺抗性时增强BPTES的作用。BCH NPs 有效根除 TNBC 肿瘤并抑制肿瘤转移,具有良好的生物相容性。

"点击查看英文标题和摘要"






























 京公网安备 11010802027423号
京公网安备 11010802027423号