当前位置:
X-MOL 学术
›
Adv. Healthcare Mater.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
A Versatile Design-Enabled Analysis of Circulating Extracellular Vesicles in Disease Diagnosis
Advanced Healthcare Materials ( IF 10.0 ) Pub Date : 2023-02-05 , DOI: 10.1002/adhm.202203119 Qi Liu 1, 2 , Jianhua Yao 3 , Zichen Huang 1 , Shuning Wang 1 , Jizong Jiang 2, 4 , Ya Cao 1 , Yihua Bei 2, 4 , Jing Zhao 1
Advanced Healthcare Materials ( IF 10.0 ) Pub Date : 2023-02-05 , DOI: 10.1002/adhm.202203119 Qi Liu 1, 2 , Jianhua Yao 3 , Zichen Huang 1 , Shuning Wang 1 , Jizong Jiang 2, 4 , Ya Cao 1 , Yihua Bei 2, 4 , Jing Zhao 1
Affiliation
|
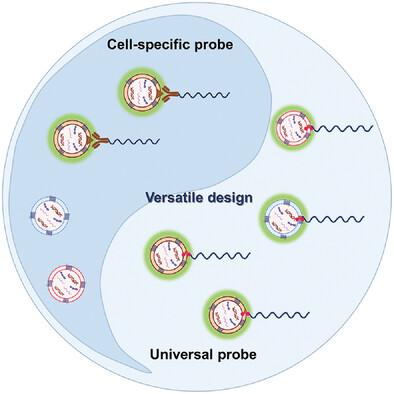
Circulating extracellular vesicles (EVs) are considered as potential biomarkers for treatment and diagnosis of many diseases. Most of the existing methods for the EV analysis only have a single function and thus reveal limited information carried by EVs. Herein, a phosphatidylserine-targeting peptide-facilitated design that enables the versatile analysis of circulating EVs for varying requirement is proposed. In the design, DNA probes are inserted into the EV membrane through hydrophobic interactions, and accelerate the removal of protective shielding from DNA-gated metal–organic framework, thereby releasing a large number of methylene blue molecules to amplify the electrochemical signal. Electrochemical results demonstrate equally high sensitivities toward the quantification of EVs derived from different cell sources using an indiscriminative DNA probe. More importantly, the probe can be endowed with extended function for more accurate classification of cell-specific features through the identification of specific EV biomarkers, and demonstrates the potential use in the diagnosis of cardiovascular in a principle-of-proof study for clinical application. Therefore, the method provides a versatile design for the identification of EV features, and may address the needs of clinical diagnosis in the future.
中文翻译:

疾病诊断中循环细胞外囊泡的多功能设计分析
循环细胞外囊泡(EV)被认为是治疗和诊断许多疾病的潜在生物标志物。大多数现有的电动汽车分析方法只有单一功能,因此揭示电动汽车携带的信息有限。在此,提出了一种磷脂酰丝氨酸靶向肽促进的设计,该设计能够根据不同的要求对循环 EV 进行多功能分析。在设计中,DNA探针通过疏水相互作用插入EV膜中,加速去除DNA门控金属有机框架的保护屏蔽,从而释放大量亚甲基蓝分子来放大电化学信号。电化学结果表明,使用无差别 DNA 探针对不同细胞来源的 EV 进行定量具有同样高的灵敏度。更重要的是,该探针可以被赋予扩展功能,通过识别特定的EV生物标志物来更准确地分类细胞特异性特征,并在临床应用的证明原理研究中展示其在心血管诊断中的潜在用途。因此,该方法为识别EV特征提供了一种通用的设计,并可能满足未来临床诊断的需求。并在临床应用的证明原理研究中展示了其在心血管诊断中的潜在用途。因此,该方法为识别EV特征提供了一种通用的设计,并可能满足未来临床诊断的需求。并在临床应用的证明原理研究中展示了其在心血管诊断中的潜在用途。因此,该方法为识别EV特征提供了一种通用的设计,并可能满足未来临床诊断的需求。
更新日期:2023-02-05
中文翻译:

疾病诊断中循环细胞外囊泡的多功能设计分析
循环细胞外囊泡(EV)被认为是治疗和诊断许多疾病的潜在生物标志物。大多数现有的电动汽车分析方法只有单一功能,因此揭示电动汽车携带的信息有限。在此,提出了一种磷脂酰丝氨酸靶向肽促进的设计,该设计能够根据不同的要求对循环 EV 进行多功能分析。在设计中,DNA探针通过疏水相互作用插入EV膜中,加速去除DNA门控金属有机框架的保护屏蔽,从而释放大量亚甲基蓝分子来放大电化学信号。电化学结果表明,使用无差别 DNA 探针对不同细胞来源的 EV 进行定量具有同样高的灵敏度。更重要的是,该探针可以被赋予扩展功能,通过识别特定的EV生物标志物来更准确地分类细胞特异性特征,并在临床应用的证明原理研究中展示其在心血管诊断中的潜在用途。因此,该方法为识别EV特征提供了一种通用的设计,并可能满足未来临床诊断的需求。并在临床应用的证明原理研究中展示了其在心血管诊断中的潜在用途。因此,该方法为识别EV特征提供了一种通用的设计,并可能满足未来临床诊断的需求。并在临床应用的证明原理研究中展示了其在心血管诊断中的潜在用途。因此,该方法为识别EV特征提供了一种通用的设计,并可能满足未来临床诊断的需求。






























 京公网安备 11010802027423号
京公网安备 11010802027423号