当前位置:
X-MOL 学术
›
Adv. Mater.
›
论文详情
Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
Photomagnetically Powered Spiky Nanomachines with Thermal Control of Viscosity for Enhanced Cancer Mechanotherapy
Advanced Materials ( IF 27.4 ) Pub Date : 2022-12-14 , DOI: 10.1002/adma.202204996 Chang Xu 1 , Yali Liu 1 , Jiayan Li 2 , Peng Ning 1 , Zhong Shi 3 , Wei Zhang 4 , Zhenguang Li 1 , Ruimei Zhou 1 , Yifan Tong 1 , Yingze Li 1 , Cheng Lv 1 , Yajing Shen 1 , Qian Cheng 2 , Bin He 4 , Yu Cheng 1
Advanced Materials ( IF 27.4 ) Pub Date : 2022-12-14 , DOI: 10.1002/adma.202204996 Chang Xu 1 , Yali Liu 1 , Jiayan Li 2 , Peng Ning 1 , Zhong Shi 3 , Wei Zhang 4 , Zhenguang Li 1 , Ruimei Zhou 1 , Yifan Tong 1 , Yingze Li 1 , Cheng Lv 1 , Yajing Shen 1 , Qian Cheng 2 , Bin He 4 , Yu Cheng 1
Affiliation
|
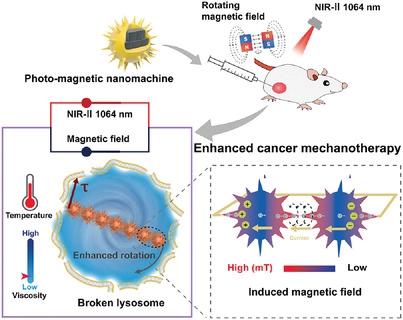
Nanomachines with active propulsion have emerged as an intelligent platform for targeted cancer therapy. Achieving an efficient locomotion performance using an external energy conversion is a key requirement in the design of nanomachines. In this study, inspired by diverse spiky structures in nature, a photomagnetically powered nanomachine (PMN) with a spiky surface and thermally dependent viscosity tunability is proposed to facilitate mechanical motion in lysosomes for cancer mechanotherapy. The hybrid nanomachine is integrated with magnetic nanoparticles as the core and covered with gold nanotips. Physical simulations and experimental results prove that the spiky structure endows nanomachines with an obvious photomagnetic coupling effect in the NIR-II region through the alignment and orienting movement of plasmons on the gold tips. Using a coupling-enhanced magnetic field, PMNs are efficiently assembled into chain-like structures to further elevate energy conversion efficiency. Notably, PMNs with the thermal control of viscosity are efficiently propelled under simultaneously applied dual external energy sources in cell lysosomes. Enhanced mechanical destruction of cancer cells via PMNs is confirmed both in vitro and in vivo under photomagnetic treatment. This study provides a new direction for designing integrated nanomachines with active adaptability to physiological environments for cancer treatment.
中文翻译:

用于增强癌症机械治疗的具有粘度热控制的光磁动力尖尖纳米机器
具有主动推进力的纳米机器已成为靶向癌症治疗的智能平台。使用外部能量转换实现高效的运动性能是纳米机器设计的关键要求。在这项研究中,受自然界中各种尖刺结构的启发,提出了一种具有尖刺表面和热依赖性粘度可调性的光磁驱动纳米机器 (PMN),以促进溶酶体中的机械运动以进行癌症机械治疗。混合纳米机器以磁性纳米粒子为核心集成,并覆盖有金纳米尖端。物理模拟和实验结果证明,尖刺结构通过等离激元在金尖上的排列和定向运动,赋予纳米机器在 NIR-II 区域明显的光磁耦合效应。使用耦合增强磁场,PMNs 被有效地组装成链状结构,以进一步提高能量转换效率。值得注意的是,具有粘度热控制的 PMN 在细胞溶酶体中同时应用双重外部能源的情况下得到有效推动。在光磁处理下,在体外和体内都证实了通过 PMN 增强对癌细胞的机械破坏。该研究为设计具有主动适应生理环境的癌症治疗集成纳米机器提供了新方向。具有粘度热控制的 PMN 在细胞溶酶体中同时应用双重外部能源的情况下得到有效推动。在光磁处理下,在体外和体内都证实了通过 PMN 增强对癌细胞的机械破坏。该研究为设计具有主动适应生理环境的癌症治疗集成纳米机器提供了新方向。具有粘度热控制的 PMN 在细胞溶酶体中同时应用双重外部能源的情况下得到有效推动。在光磁处理下,在体外和体内都证实了通过 PMN 增强对癌细胞的机械破坏。该研究为设计具有主动适应生理环境的癌症治疗集成纳米机器提供了新方向。
更新日期:2022-12-14
中文翻译:

用于增强癌症机械治疗的具有粘度热控制的光磁动力尖尖纳米机器
具有主动推进力的纳米机器已成为靶向癌症治疗的智能平台。使用外部能量转换实现高效的运动性能是纳米机器设计的关键要求。在这项研究中,受自然界中各种尖刺结构的启发,提出了一种具有尖刺表面和热依赖性粘度可调性的光磁驱动纳米机器 (PMN),以促进溶酶体中的机械运动以进行癌症机械治疗。混合纳米机器以磁性纳米粒子为核心集成,并覆盖有金纳米尖端。物理模拟和实验结果证明,尖刺结构通过等离激元在金尖上的排列和定向运动,赋予纳米机器在 NIR-II 区域明显的光磁耦合效应。使用耦合增强磁场,PMNs 被有效地组装成链状结构,以进一步提高能量转换效率。值得注意的是,具有粘度热控制的 PMN 在细胞溶酶体中同时应用双重外部能源的情况下得到有效推动。在光磁处理下,在体外和体内都证实了通过 PMN 增强对癌细胞的机械破坏。该研究为设计具有主动适应生理环境的癌症治疗集成纳米机器提供了新方向。具有粘度热控制的 PMN 在细胞溶酶体中同时应用双重外部能源的情况下得到有效推动。在光磁处理下,在体外和体内都证实了通过 PMN 增强对癌细胞的机械破坏。该研究为设计具有主动适应生理环境的癌症治疗集成纳米机器提供了新方向。具有粘度热控制的 PMN 在细胞溶酶体中同时应用双重外部能源的情况下得到有效推动。在光磁处理下,在体外和体内都证实了通过 PMN 增强对癌细胞的机械破坏。该研究为设计具有主动适应生理环境的癌症治疗集成纳米机器提供了新方向。































 京公网安备 11010802027423号
京公网安备 11010802027423号