Our official English website, www.x-mol.net, welcomes your
feedback! (Note: you will need to create a separate account there.)
用于 PD1/PDL1 轴阻断和增强免疫治疗的基于双特异性适配体的识别然后结合策略
ACS Nano ( IF 15.8 ) Pub Date : 2022-12-09 , DOI: 10.1021/acsnano.2c09093
Yang Sun 1 , Liuting Mo 2 , Xiaoxiao Hu 2 , Die Yu 1 , Sitao Xie 3 , Jianglin Li 2 , Zilong Zhao 2 , Xiaohong Fang 3 , Mao Ye 2 , Liping Qiu 2 , Weihong Tan 1, 2, 3 , Yu Yang 1
ACS Nano ( IF 15.8 ) Pub Date : 2022-12-09 , DOI: 10.1021/acsnano.2c09093
Yang Sun 1 , Liuting Mo 2 , Xiaoxiao Hu 2 , Die Yu 1 , Sitao Xie 3 , Jianglin Li 2 , Zilong Zhao 2 , Xiaohong Fang 3 , Mao Ye 2 , Liping Qiu 2 , Weihong Tan 1, 2, 3 , Yu Yang 1
Affiliation
|
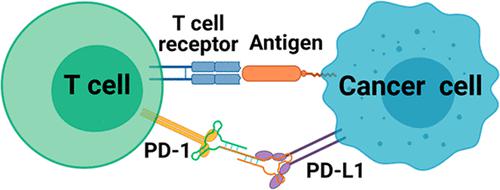
细胞毒性 T 细胞主要通过与肿瘤细胞的直接相互作用来启动抗肿瘤作用。与此相反,肿瘤细胞可以通过程序性死亡配体 1 (PDL1) 及其受体程序性细胞死亡蛋白 1 (PD1) 之间的特定连接来抑制这种 T 细胞活性。双特异性抑制剂能够同步阻断 PD1 和 PDL1,从而释放对 T 细胞抗肿瘤活性的抑制,应该会显着提高免疫检查点阻断 (ICB) 疗法的疗效。在这项工作中,我们鉴定了一种 DNA 适体 Ap3,它可以特异性识别肿瘤细胞上的 PDL1,并与 PD1 竞争结合。通过将 Ap3 与抗 PD1 适配体整合,构建了双特异性适配体 Ap3-7c,并有望改善 T 细胞免疫反应。我们进一步设计了二苯并环辛炔 (DBCO) 标记的双特异性适配体 D-Ap3–7c,允许适配体在特异性细胞识别后共价结合到 PD1 和 PDL1 上。我们的体内研究表明,这种先识别后结合的策略可以诱导针对肿瘤的强大免疫效应。这项工作有望为抗肿瘤免疫治疗提供线索。

"点击查看英文标题和摘要"
更新日期:2022-12-09

"点击查看英文标题和摘要"


































 京公网安备 11010802027423号
京公网安备 11010802027423号